
科目: 来源: 题型:
化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1) 催化反硝化法中,H2能将NO3—还原为N2,25℃时,反应进行10min,溶液的pH由7变为12。
①N2的结构式为 。
②上述反应离子方程式为 ,其平均反应速率v(NO3—)为 。
|
④在NaNO2 溶液中,质子守恒表达式为
___________________________________________。
(2)电化学降解NO3—的原理如右图所示。
| |
阴极反应式为:
。
查看答案和解析>>
科目: 来源: 题型:
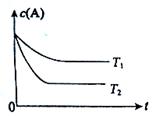
反应A(g) ![]() B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如右图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如右图所示。回答下列问题:
(1)上述反应的温度T1 T2,平衡常数K(T1) K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:①平衡时体系总的物质的量为 。 ②反应的平衡常数K= 。
③反应在0~5min区间的平均反应速率v(A)= 。
查看答案和解析>>
科目: 来源: 题型:
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 。
(3)Y 与Z 可形成YZ42-
① YZ42-的空间构型为 (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式: 。
 (4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
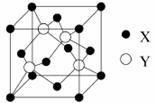
(5)X与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,X离子的数目为 。
②该化合物的化学式为 。
③已知该化合物晶体的晶胞边长为a cm,阿伏伽德罗常数为NA mol-1,则该晶体密度为____________________________g·cm-3(列出表达式即可)。
查看答案和解析>>
科目: 来源: 题型:
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:
2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为
A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 0.8 mol
查看答案和解析>>
科目: 来源: 题型:
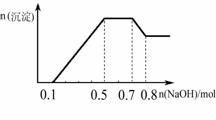
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32−、SO42−、NO3−中的几种。①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如右图所示。则下列说法正确的是
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH4+)=0.2 mol
C.溶液中一定不含CO32−,一定含有SO42−和NO3-
D.三种离子的物质的量之比n(H+)∶n(Al3+)∶n(Mg2+)= 1∶1∶1
查看答案和解析>>
科目: 来源: 题型:
某工业生产经过以下转化步骤:
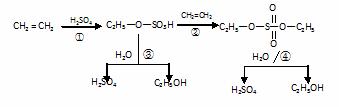
下列说法中不正确的是
A.该过程中③、④是酯类的水解反应 B.该过程中硫酸是催化剂
C.该过程中①、②是加成反应 D.该过程是一种新的硫酸生产方法
查看答案和解析>>
科目: 来源: 题型:
根据图示判断下列叙述符合事实的是

A.按图①连接并放置一段时间后,![]() 片表面会“镀”上一层铜
片表面会“镀”上一层铜
B.按图②连接好导线后(![]() 片与
片与![]() 片相接触),灵敏电流表会发生非常明显的偏转
片相接触),灵敏电流表会发生非常明显的偏转
C.按图③连接并放置片刻,在![]() 片附近加一滴
片附近加一滴![]() 溶液,溶液变为深红色
溶液,溶液变为深红色
D.按图④连接并放置一段时间后,在![]() 片上有无色气泡聚集
片上有无色气泡聚集
查看答案和解析>>
科目: 来源: 题型:
关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有Cl—存在
B.加入几滴Fe2(SO4)3溶液,溶液变成紫色,可确定有酚羟基存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在
查看答案和解析>>
科目: 来源: 题型:
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下:
| 物质 | AgCl | AgI | Ag2S |
| 颜色 | 白 | 黄 | 黑 |
| KSP(25℃) | 1.8×10-10 | 1.5×10-16 | 1.8×10-50 |
下列叙述不正确的是
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
C.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2 溶液中的溶度积相同
查看答案和解析>>
科目: 来源: 题型:
可逆反应A(g)+3B(g)![]() 2C(g) ΔH=-QkJ/mol。有甲、乙两个容积相同且不变的密闭容
2C(g) ΔH=-QkJ/mol。有甲、乙两个容积相同且不变的密闭容
器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相
同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2。下列叙述
不正确的是
A.甲中A的转化率为75% B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向正向移动
D.乙中的热化学方程式为2C(g)![]() A(g)+3B(g) ΔH= +Q2 kJ/mol
A(g)+3B(g) ΔH= +Q2 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com