
科目: 来源: 题型:
将0.1 mol N2O4置于密闭烧瓶中,把烧瓶放入100 ℃的恒温水浴,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g),能说明反应在该条件下达到平衡的是( )
2NO2 (g),能说明反应在该条件下达到平衡的是( )
① N2O4的消耗速率与NO2的生成速率之比为1∶2;
② 烧瓶内气体的质量和密度不再变化;
③烧瓶内气体的压强不再变化;
④烧瓶内气体的平均相对分子质量不再变化
A.①② B.②③ C.③④ D.②③④
查看答案和解析>>
科目: 来源: 题型:
在0.10mol·L-1NH3·H2O溶液中,加入少量NH4Cl晶体后,引起的变化是( )
A.NH3·H2O的电离程度减小 B.NH3·H2O的电离常数增大
C.溶液的导电能力不变 D.溶液的pH增大
查看答案和解析>>
科目: 来源: 题型:
在2A﹢B![]() 2C﹢D反应中,表示该反应速率最快的是( )
2C﹢D反应中,表示该反应速率最快的是( )
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:
2NO2 + Na2CO3 → NaNO2 + NaNO3 + CO2↑ ①
NO + NO2 + Na2CO3 → 2NaNO2 + CO2↑ ②
⑴ 根据反应①,每产生22.4L(标准状况下)CO2,吸收液质量将增加___________g。
⑵配制1000g 质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O g。
⑶ 现有1000g 质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4L(标准状况下)CO2时,吸收液质量就增加44g。
①吸收液中NaNO2 和NaNO3 的物质的量之比
② 1000g 质量分数为21.2%的纯碱在20℃经充分吸收硝酸工业尾气后,蒸发掉688g水,冷却到0℃,最多可析出NaNO2 克(0℃时,NaNO2的溶解度为71.2g/100g水)
查看答案和解析>>
科目: 来源: 题型:
某同学用如图所示装置制取溴苯和溴乙烷。已知溴乙烷为无色液体,难溶于水,沸点为38.4℃,熔点为-119℃,密度为1.46 g·cm-3。
![]()

主要实验步骤如下:
①检查装置的气密性后,向烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓H2SO4的混合液至稍高于进气导管口处。
③将A装置中的纯铁丝小心向下插入混合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10 min。
请填写下列空白:
(1)A中制取溴苯的化学方程式_________________________________。
(2)导管a的作用是___________________________________。
(3)C装置中U形管内部用蒸馏水封住管底的作用是
___________________________________________________________________。
(4)反应完毕后,分离U形管内溴乙烷所用的最主要仪器的名称是(只填一种)_________。
(5)步骤④中能否用大火加热,理由是___________________________________。
(6)为证明溴和苯的上述反应是取代反应而不是加成反应,该同学用装置D代替装置B、C直接与A相连重新操作实验。D中小试管内CCl4作用 ;
还需使用的试剂是 ;
查看答案和解析>>
科目: 来源: 题型:阅读理解
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
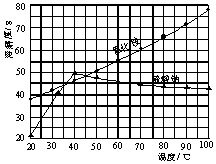
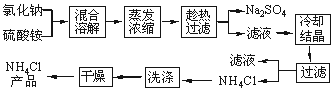
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)写出制备 NH4Cl的化学方程式: 。
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
 (3)实验过程中趁热过滤的目的是 。趁热过滤可采用抽滤装置,抽滤装置如图1所示,该装置中的错误之处是 ;若用普通的漏斗,贴上滤纸后,接上抽滤瓶进行吸滤则不行,因为 。
(3)实验过程中趁热过滤的目的是 。趁热过滤可采用抽滤装置,抽滤装置如图1所示,该装置中的错误之处是 ;若用普通的漏斗,贴上滤纸后,接上抽滤瓶进行吸滤则不行,因为 。
![]() (布氏漏斗的使用:一般先在圆筒底面垫上滤纸,将布氏漏斗插进抽滤瓶并将接口密封。抽滤瓶的侧口连抽气系统。然后将欲分离的固体、液体混合物倒进上方,液体成分在负压力作用下被抽进抽滤瓶中,固体留在上方。)
(布氏漏斗的使用:一般先在圆筒底面垫上滤纸,将布氏漏斗插进抽滤瓶并将接口密封。抽滤瓶的侧口连抽气系统。然后将欲分离的固体、液体混合物倒进上方,液体成分在负压力作用下被抽进抽滤瓶中,固体留在上方。)

图1 图2
(4)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体____。
A.缓慢冷却溶液 B.溶液浓度较高 C.溶质溶解度较小 D.缓慢蒸发溶剂
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是 ___。某研究性学习小组为测定该NH4Cl产品中氮的含量,设计了如图2装置,并进行了讨论。
甲同学:根据此实验测得的数据,计算的NH4Cl产品的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:__ ____。
乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液一定要足量并充分加热,原因是 。
用改进后的实验装置重新进行实验,称取13.5gNH4Cl产品,测得实验后B装置增重3.4g。则该化肥含氮量为 。
查看答案和解析>>
科目: 来源: 题型:
某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:
①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氨水,产生白色沉淀,过滤;
③向②所得的滤液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
④向③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子是 ;
(2)原溶液中可能存在的离子是 。为检验该离子是否存在,应补充的实验为(写出实验过程): 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com