
科目: 来源: 题型:
下列反应的离子方程式正确的是
A.溶质物质的量相等的Ba(OH)2与KAl(SO4)2·12H2O溶液混合:
Ba2++6OH-+2Al3++SO![]() ===BaSO4↓+2Al(OH)3↓
===BaSO4↓+2Al(OH)3↓
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO![]() +CO2+2H2O===Al(OH)3↓+HCO
+CO2+2H2O===Al(OH)3↓+HCO![]()
D.将适量CO2通入Ca(ClO) 2溶液中:2ClO-+CO2+H2O===CO![]() +2HClO
+2HClO
查看答案和解析>>
科目: 来源: 题型:
下列关于有机物的说法中,正确的一组是
①淀粉、油脂、蛋白质在一定的条件下都能发生水解反应
②“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
③除去乙酸乙酯中残留的乙酸,可加过量饱和碳酸钠溶液振荡后,静置分液
④石油的分馏、裂化和煤的干馏都是化学变化
⑤淀粉遇碘酒变蓝色,葡萄糖能与新制氢氧化铜溶液反应
⑥汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成CO2和H2O
A.①③⑤ B.②④⑥ C. ①②⑤ D. ③④⑥
查看答案和解析>>
科目: 来源: 题型:
有关粒子在相应条件下可大量共存的是
A.常温常压下混合气体:H2、F2、NO、O2
B.pH=14的溶液中:Na+、K+、SO42-、 CO32-
C.c(H+)=1.0 mol·L-1的溶液中:K+、Fe3+、SO42-、I-
D.含有0.1 mol·L-1Ca2+的溶液中:Na+、Cu2+、SiO32-、NO3-
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.浓硫酸可用于干燥氢气、碘化氢等气体,但不能干燥氨气、二氧化氮气体
B.将SO2通入溴水中,能使溴水褪色体现了SO2的还原性
C.MgCl2、AlCl3溶液中分别加入过量的氨水来比较镁、铝的金属性强弱
D.含FeCl3、CuCl2溶液中加入铁粉,充分反应后有固体剩余,加入KSCN溶液呈血红色
查看答案和解析>>
科目: 来源: 题型:
化学已渗透到人类生活的各个方面。下列说法正确的是
A.为防止富脂食品氧化变质,常在包装袋中放入生石灰
B.铬是人体必需的微量元素,但铬过量会危害人体健康,其中六价铬的毒性最大。人体内六价铬超标,可以服用维生素C缓解毒性,说明维生素C具有氧化性
C.去年冬天的雾霾天气严重影响了人们的正常出行和生活节奏。为改善空气质量,可以加高工厂的烟囱,使烟尘和废气远离地表
D.禁止使用四乙基铅作汽油抗爆震剂,可减少环境中的铅污染
查看答案和解析>>
科目: 来源: 题型:
可逆反应A(g)+ B(g)![]() C(g)在两个容积相等的甲、乙容器中分别加入A、B各1mol,甲容器在500℃时达到平衡,压强为原来的75%,乙容器在700℃时达到平衡,B的转化率为30%。
C(g)在两个容积相等的甲、乙容器中分别加入A、B各1mol,甲容器在500℃时达到平衡,压强为原来的75%,乙容器在700℃时达到平衡,B的转化率为30%。
(1)计算甲容器中A的转化率。
(2)判断该反应的正方向是放热反应还是吸热反应。
查看答案和解析>>
科目: 来源: 题型:
在T ℃条件下,向1 L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:
2X(g)+Y(g) ![]() a Z(g)+W(g) ΔH=-Q kJ·mol-1(Q>0,a为正整数)。
a Z(g)+W(g) ΔH=-Q kJ·mol-1(Q>0,a为正整数)。
当反应达到平衡后,反应放出的热量为Q1 kJ,若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为________。
(2)下列说法中能说明该反应达到了化学平衡状态的是________。
A.容器内压强一定 B.容器内气体的密度一定
C.容器内Z分子数一定 D.容器内气体的质量一定
E.容器内气体的平均相对分子质量不再变化
(3)温度维持T ℃不变,若起始时向容器M中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是________(稀有气体不参与反应)。
A.2 mol X、1 mol Y、1 mol Ar
B.a mol Z、1 mol W
C.1 mol X、0.5 mol Y、0.5a mol Z、0.5 mol W
D.2 mol X、1 mol Y、1 mol Z
(4)已知:该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
若在某温度下,2 mol X和1 mol Y在容器M中反应达平衡, X的平衡转化率为50%,则该温度为________℃。ks5u
查看答案和解析>>
科目: 来源: 题型:
(1)有甲、乙两容器,甲的容积固定,乙的容积可变。在一定温度下,向甲中通入3molN2和4molH2,反应达到平衡时,生成NH3物质的量为amol。
①相同温度下,若乙中通入6molN2和8molH2,且保持压强与甲相同,反应达到平衡时,生成NH3物质的量为bmol,则b与a的关系可表示为__________ ,两容器中氮气的转化率甲____乙(填“>”、“<”或“=”)
②若①中乙与甲的容积始终相等,达到平衡时,生成NH3物质的量为Cmol,则C与a的关系可表示为___________
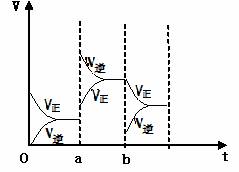
(2)下图左表示在密闭容器中反应:2SO2+O2![]() 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
a 时刻改变的条件可能是 ;
b 时刻改变的条件可能是 ;
查看答案和解析>>
科目: 来源: 题型:
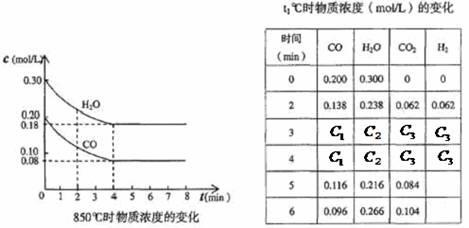
(1) 在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应: CO(g)十H2O(g)![]() CO2(g)十H2(g) ΔH < 0, CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L·min)
CO2(g)十H2(g) ΔH < 0, CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L·min)
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。
①表中3 min~4 min之间反应处于_________状态;C1数值_________0.08 mol/L (填大于、小于或等于)。ks5u
②反应在4 min~5 min之间,平衡向逆方向移动,可能的原因是_______(单选),表中5 min~6 min之间数值发生变化,可能的原因是_______(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com