
科目: 来源: 题型:
下列叙述中正确的是 ( )
A.1mol任何纯净物都含有相同的分子数
B.1molO2中约含有6.02×1023个氧分子
C.1mol氢中含有2mol氢原子
D.阿伏加德罗常数就是6.02×1023mol-1
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试计算:
(1)O2的转化率为 ?
( 2)用SO2表示该反应的反应速率为 ?
( 3)平衡常数K为 ?
查看答案和解析>>
科目: 来源: 题型:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液
在如图所示的装置中进行中和反应。通过测定反应过程中所放
出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 (1分)。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (1分)(填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的
热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;
(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
在一固定体积的密闭容器中,在900℃时发生反应:
CH4(g)+H2O(g)![]() CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
| 时间/min | CH4 | H2O | CH3OH | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是 。
A.容器内压强不变 B.v正(H2)=v逆(CH4)
C.混合气体中CH3OH的浓度不变 D.c(CH3OH)=c(CH4)
(2)若在900℃时向反应容器中充入H2O,K值 (填“增大”“减小”或“不变”,下同);若升高反应体系的温度,K值 。
(3)上表中:c1= mol/L,H2O的转化率为 。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.下图是表示在密闭容器中反应:2SO2+O2![]() 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
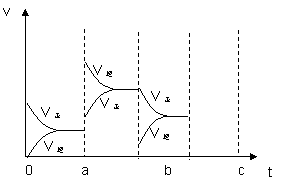 |
查看答案和解析>>
科目: 来源: 题型:
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________________________ 。
(2)(6分)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气, 已知
N2(g)+2O2(g)=2NO2(g) ⊿ H1 = + 67.7kJ/mol;
N2H4(g)+O2(g)= N2(g)+2H2O(g) ⊿ H2 = - 534kJ/mol;
2H2(g)+ O2(g)= 2H2O (g) ⊿ H3 = - 484kJ/mol;
H2(g)+F2(g)=2HF(g) ⊿ H4 = - 538kJ/mol
写出N2H4与 NO2反应的热化学方程式________________________________________,
写出N2H4与F2反应的热化学方程式__________________________________________
查看答案和解析>>
科目: 来源: 题型:
①CaCO3(s) == CaO + CO2(g) ΔH = 177.7kJ/mol
②2H2(g) + O2(g) == 2H2O(l) ΔH = -517.6kJ
③0.5H2SO4(l) + NaOH(l) == 0.5Na2SO4(l) + H2O(l) ΔH = -57.3kJ/mol
④C(s) + O2(g) == CO2(g) ΔH =-393.5kJ/mol
⑤CO(g) + 1/2 O2(s) == CO2(g) ΔH =-283kJ/mol
⑥HNO3 (aq) + NaOH(aq) == NaNO3(aq) + H2O(l) ΔH = -57.3kJ/mol
(1)上述热化学方程式中,共有 个不正确的,并分别指明不正确的理由___________________________ ;
(2)根据上述信息,写出C转化为CO的热化学方程式______________________________。
(3)上述反应中,表示燃烧热的热化学方程式有 ;表示中和热的热化学方程式有
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com