
科目: 来源: 题型:
铅蓄电池用处极广,可多次充放电。铅蓄电池中铅作负极,二氧化铅作正极,电解
液为30%H2SO4溶液。电池充、放电时的总反应可表示为2PbSO4+2H2O![]() Pb+PbO2+2H2SO4下列关于此电池的说法中,不正确的是( )
Pb+PbO2+2H2SO4下列关于此电池的说法中,不正确的是( )
A放电一段时间后,电解液的pH将增大
B充电时,电解液中的阳离子向二氧化铅电极移动
C放电时,铅电极上发生的电极反应为:Pb+SO42-→PbSO4+2e-
D充电时,两极的量均减少,氧化铅电极发生氧化反应。
查看答案和解析>>
科目: 来源: 题型:
金属镍有广泛的用途。粗镍中含有少量的Fe、Cu、Zn、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
A阳极发生还原反应,其电极反应式为Ni2++2e-=Ni
B电解过程中,阳极质量的减少和阴极质量的增加相等
C电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D电解后,电解槽底部的阳极泥只有Cu和Pt
查看答案和解析>>
科目: 来源: 题型:
pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的 pH>a,
则电解质可能是( )
A NaOH B H2SO4 C AgNO3 D Na2SO4
查看答案和解析>>
科目: 来源: 题型:
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):
H2(g)+Cl2(g)==2HCl(g)+Q1 H2(g)+Br2(g)==2HBr(g)+Q2
有关上述反应的叙述正确的是( )
A.Q1>Q2
B.生成物总能量均高于反应物总能量
C.生成1 mol HCl气体时放出Q1热量
D.1 mol HBr(g)具有的能量小于1 mol HBr(l)具有的能量
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.工业上电解熔融的Al2O3冶炼铝用铁做阳极
B.用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1molNaOH
D.用惰性电极电解CuSO4溶液一段时间后,加入Cu(OH)2固体可以使CuSO4溶液恢复原来浓度
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A 任何酸和碱发生中和反应生成1molH2O的过程中,能量变化均相同
B 已知:C(s,石墨)=C(s,金刚石) ∆H=1.5kJ·mol-! , 则金刚石比石墨更稳定
C 若①2H2(g)+O2(g)=2H2O(g) ∆H=-a kJ·mol-!
②2H2(g)+O2(g)=2H2O(l) ∆H=-b kJ·mol-! 则 b>a
D 放热反应不需要任何条件就能发生
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式书写正确的是( )
A 2SO2+O2![]() 2SO3 ∆H=-196.6kJ·mol-!
2SO3 ∆H=-196.6kJ·mol-!
B 4H2(g)+2O2(g)=4H2O(l) ∆H=-1143.2kJ·mol-!
C C(s)+O2(g)=CO2(g) ∆H=393.5kJ
D C(s)+O2(g)=CO2(g) ∆H=393.5kJ·mol-!
查看答案和解析>>
科目: 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目: 来源: 题型:
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:

已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(1)化合物FeTiO3中铁元素的化合价是 。
(2)滤渣A的成分是 。
(3)滤液B中TiOCl42- 转化生成TiO2的离子方程式是 。
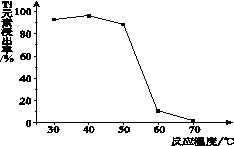
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如 下图所示。反应温度过高时,Ti元素浸出率下降的原因是 。
(5)反应③的化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com