
科目: 来源: 题型:
用NA表示阿伏伽德罗常数的值。下列叙述正确的是:( )
A.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
B.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4L甲醇中含有的氧原子数为1.0NA
查看答案和解析>>
科目: 来源: 题型:
下列各组离子中,能大量共存,溶液呈现无色,且加入一小块钠粒后仍然能大量共存 ( )
A.K+、MnO4—、SO42—、H+ B.Ba2+、Na+、HCO3—、NO3—
C.Na+、NO3—、K+、Cl— D.Ca2+、NO3—、Cl—、CO32—
查看答案和解析>>
科目: 来源: 题型:
用NaOH固体配制1.0 mol·L-1的NaOH溶液220mL,下列说法正确的是( )
A.首先称取NaOH固体8.8g
B.容量瓶中原有少量蒸馏水没有影响
C.定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线
D.定容时仰视刻度线会使所配制的溶液浓度偏高
查看答案和解析>>
科目: 来源: 题型:
NA代表阿伏加德罗常数的值,以下说法正确的是( )
A.2NA个HCl分子与44.8L H2和Cl2的混合气体所含的原子数目均为4NA
B.32gCu将浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA
C.物质的量浓度均为1mol·L-1的NaCl和MgCl2混合溶液中,含有Cl-的数目为3NA
D.将NA个Cl2分别通入到足量的水和NaOH溶液中,此时所转移的电子总数均为NA
查看答案和解析>>
科目: 来源: 题型:
在一含Na+的澄清溶液中,可能还存在NH4+、Fe2+、I![]() 、Br
、Br![]() 、CO32-、SO32-种离子中的几种。①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈黄色;②向呈黄色的溶液中加入BaCl2溶液时无沉淀生成;③黄色溶液不能使淀粉溶液变蓝色。根据上述实验事实推断,下列说法不正确的是 ( )
、CO32-、SO32-种离子中的几种。①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈黄色;②向呈黄色的溶液中加入BaCl2溶液时无沉淀生成;③黄色溶液不能使淀粉溶液变蓝色。根据上述实验事实推断,下列说法不正确的是 ( )
A.溶液中一定存在Br-、CO32-
B.溶液中可能存在NH4+
C.溶液中一定不存在Fe2+、I-、SO32--
D.溶液一定呈碱性
查看答案和解析>>
科目: 来源: 题型:
将下列A~D四组物质wg分别在O2中充分燃烧后,再通过装有足量Na2O2的干燥管,干燥管增重的质量大于wg的是( )
A.C4H8O2 B.C6H12O6
C.C2H4O3 D.H2和CO的混合气体
查看答案和解析>>
科目: 来源: 题型:
科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法错误的是( )
A.该原子的摩尔质量是aNA g/mol
B.该原子的相对原子质量为![]()
C.w g该原子的物质的量是![]() mol
mol
D.由已知信息可得:NA =![]() mol-1
mol-1
查看答案和解析>>
科目: 来源: 题型:
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是 ( )
A.两种气体的压强相等 B.O2比O3质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
查看答案和解析>>
科目: 来源: 题型:
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
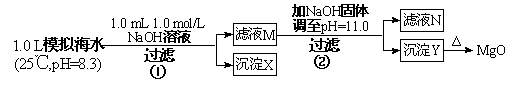
| 模拟海水中的离子 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 浓度(mol/L) | 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.84×10-6;Ksp[Mg(OH)2]=5.61×10-12。
(1)沉淀物X的化学式为 ,生成X的离子方程式 。
(2)滤液N中存在的阳离子除Na+外还有 其物质的量浓度为 mol/L。
(3)若使2处pH为11,则需加入氢氧化钠固体质量为 g;(保留三位有效数字)
若使Y为纯净物,则2处加入氢氧化钠的质量最大值为 g. (保留三位有效数字)
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是 ,E是 ;
(2)用水稀释0.1 mol·L-1B时,溶液中随着水量的增加而减小的是 (填写序号)
a.![]() b.
b.![]() c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)
 (3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是________(填写序号)
(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是________(填写序号)
a.反应所需要的时间E>A
b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E
d.E溶液里有镁粉剩余
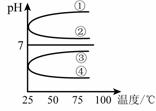
(4)将等体积、等物质的量浓度B和C混合后溶液,升高
温度(溶质不会分解)溶液pH随温度变化如右图中
_________曲线(填写序号) 。
(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com