
科目: 来源: 题型:
在一恒容密闭烧瓶中,25℃时存在平衡:2NO2(g) ![]() N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是
N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是
A. 颜色 B. 密度 C. N2O4的浓度 D. 压强
查看答案和解析>>
科目: 来源: 题型:
在恒温恒容条件下,能使反应:A(g)+B(g) ![]() C(g)+D(g)的正反应速率增大的是
C(g)+D(g)的正反应速率增大的是
A. 减小C的浓度 B.减小D的浓度 C. 减小B的浓度 D.增大A的浓度
查看答案和解析>>
科目: 来源: 题型:
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+ O2(g)===2H2O(l) △H = ―285.8 kJ·mol-1
B.2H2(g)+ O2(g)===2H2O(1) △H = +571.6 kJ·mol-1
C.2H2(g)+ O2(g)=== 2H2O(g) △H = ―571.6 kJ·mol-1
D.2H2(g)+ O2(g) === 2H2O(1) △H = ―571.6 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知在25℃、101kPa条件下,反应:N2O5(g)==4NO2(g)+O2(g) △H=+56.7
kJ·mol-1能自发进行的合理解释是
A、该反应是的熵变效应大于焓变效应 B、该反应是熵减反应
C、该反应是分解反应 D、该反应的焓变效应大于熵变效应
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.放热反应在常温下都能发生
B.放热反应一定比吸热反应的反应速率快
C.若某可逆反应的正反应放热,则逆反应一定是吸热
D.吸热反应在任何条件下都不能自发进行
查看答案和解析>>
科目: 来源: 题型:
为减少汽车对城市大气的污染,近年来中国成功开发出了以新燃料作能源的“绿色汽车”。这种汽车可避免有毒的有机铅、苯和苯的同系物及多环芳烃的排放,保护环境。该“绿色汽车”的燃料是
A.甲醇 B.汽油 C.柴油 D.重油
查看答案和解析>>
科目: 来源: 题型:
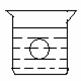 如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。(4分)(硫酸、氢氧化钡及盐溶液的密度均大于1)
如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应[设H2SO4和Ba(OH)2溶液密度相同]。(4分)(硫酸、氢氧化钡及盐溶液的密度均大于1)
试回答
⑴此实验中,观察到的现象有
① ,
② 。
⑵写出实验过程中反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
I、配制480 mL 0、3mol/L NaOH溶液。具体如下:
(1)需 gNaOH。
(2)配制过程中,下列仪器不会用到的是_____________,尚缺少的玻璃仪器是______________。
A.托盘天平 B.250mL容量瓶 C.玻璃棒 D.胶头滴管
(3) 实验过程中两次用到玻璃棒,其作用分别是:_____________________、_________________________。
(4) 定容操作:将蒸馏水注入所选的容器中,直到其中液面接近其刻度线
处时,改用 滴加蒸馏水至溶液的 正好与刻度线 。将瓶塞子盖好,反复 摇匀。
(5)下列操作的正确顺序是(用字母表示) B→ → → → → →G 。
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.转移 G.摇匀
II、乙同学用18.4mol/l浓硫酸配制100ml 3.6mol/L的稀硫酸。
用100 ml 量筒量取20 ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处
。
III、在配制物质的量浓度溶液时,下列操作出现的后果是(填:“溶液浓度不准确”、“偏低”、“偏高”、“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。_____________。
(2)配制氢氧化钠溶液时,容量瓶中有少量水。______________。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线____________。
(4) 转移时不慎将溶液倒在瓶外; ;
(5)定容时俯视容量瓶刻度线: 。
查看答案和解析>>
科目: 来源: 题型:
(1)标准状况下:22g CO2的体积是 ,其中所含分子数与 gO2相同。
(2)0.01 mol某气体的质量是0.28g,该气体的摩尔质量是 ;
(3)相同条件下,CH4与O2的质量比是1:8时二者的体积比是 。
(4)2gNaOH溶于水配制成 mL溶液时其物质的量浓度为2mol/L。
(5)标准状况下,把2.24LHCl气体溶于水,配制成250mL溶液,则该溶液的物质的量浓度为 ,若其密度为1.1g/mL,则其溶质的质量分数是
%。
查看答案和解析>>
科目: 来源: 题型:
(1)下列物质: ⑴Na⑵ Br2 ⑶Na2O ⑷NO2 ⑸CO2 ⑹ SO3 ⑺NH3 ⑻H2S ⑼HCl ⑽ H2SO4 ⑾Ba(OH)2 ⑿NaCl ⒀蔗糖 ⒁NaCl溶液。
属于电解质的是 , 属于非电解质的是 ,
能导电的是 。
(2)在Fe3O4 +4CO![]() 3Fe+4CO2的的中, 是氧化剂, 元素被氧化。
3Fe+4CO2的的中, 是氧化剂, 元素被氧化。
(3)写出下列物质的电离方程式:
NaHSO4 ,
H2SO4 ,
NH4HCO3 。
(4)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:
先出现 ,原因:
,随后
。原因(用离子方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com