
科目: 来源: 题型:
设NA表示阿伏加德罗常数,下列说法正确的是
A.在常温常压下,11.2L N2含有的分子数为0.5NA
B.在常温常压下,18 g水中含有的分子数为NA
C.含有分子数为NA的氧气的质量是32g/mol
D.在2mol/L的MgCl2溶液中含有的Cl- 数为4NA
查看答案和解析>>
科目: 来源: 题型:
下列物质属于电解质的一组是
A.CO2、NH3、HCl B.H2SO4、HNO3、BaCl2
C.H2SO4、H2O、Cu D.液态KNO3、NaOH溶液、CH3CH2OH
查看答案和解析>>
科目: 来源: 题型:阅读理解
某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末各组分均能被磁铁吸引。查阅资料得知:在温度不同、受热不均时会生成具有磁性的Fe3O4(组成相当于Fe2O3•FeO)。为进一步探究黑色粉末的组成及含量,他们进行了如下实验。
一.定性检验
(1)往黑色粉末中滴加盐酸,发现有气泡产生,则黑色粉末中一定有_ ___,产生气泡的离子方程式为____ 。
(2)热还原法检验:按下图装置连接好仪器(图中夹持设备已略去),检查装置的气密性。往装置中添加药品。打开止水夹K通人氢气,持续一段时间后再点燃C处的酒精灯。
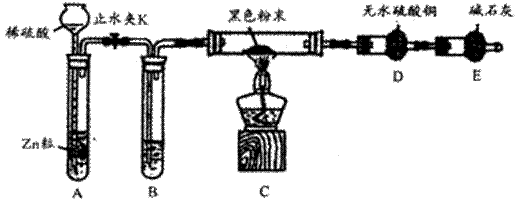
请回答下列问题:
①点燃C处酒精灯之前,为何要先持续通H2一段时间 。
②B中试剂的名称是_ 。
③若加热一段时间后,装置D中白色粉末变蓝色,对黑色粉末的组成得出的结论是 。
(3)为证明黑色粉末是否含Fe3O4,某同学还进行了如下实验:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,所得溶液分两份,第一份溶液滴入KSCN溶液,观察溶液是否变红;第二份溶液滴入酸性KMnO4溶液,观察酸性KMnO4溶液是否褪色。请回答:第一份溶液滴入KSCN溶液后一定会变红吗?请结合离子方程式简答 ;第二份溶液所进行的操作是欲检验溶液中是否存在 离子。经分析,你认为此方案是否可行 (填“是”或“否”)。
二.沉淀法定量测定
按如下实验流程进行测定:
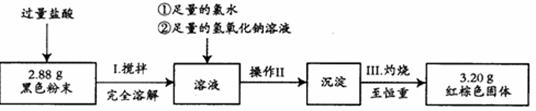
(4)操作II的名称是________ 、 ____ 、转移固体。
(5)通过以上数据,计算黑色粉末中各组分的物质的量之比为 。
查看答案和解析>>
科目: 来源: 题型:
锂离子电池的广泛应用使回收利用锂资源成为重要课题。某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4和碳粉涂覆在铝箔上)进行资源回收研究,设计实验流程如下:

(1)第①步中生成气体的反应离子方程式为 ;第②步反应得到的沉淀X的化学式为 。
(2)第③步反应有锂离子(Li+)生成,其反应的离子方程式是 。
(3)四步实验都包含过滤,实验室中过滤实验要使用的玻璃仪器包括
。
(4)若废旧锂离子电池的正极材料含LiMn2O4质量为18.1g,第③步反应中加入20.0mL 3.0mol·L-1的H2SO4溶液,假定正极材料中的锂经反应③和④完全转化为Li2CO3,则至少有 g Na2CO3参加了反应。
查看答案和解析>>
科目: 来源: 题型:
科学家利用Na2CO3溶液喷淋捕捉空气中CO2,设计技术流程如图1:

请回答下列问题:
(1)Na2CO3溶液喷成雾状的目的是____ 。
(2)在500℃的反应炉中发生反应的化学方程式为 。
(3)在整个流程中,可以循环利用的物质是 。
 (4)为研究合成塔反应最佳条件,在10 L密闭
(4)为研究合成塔反应最佳条件,在10 L密闭
容器中发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
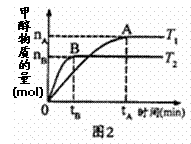
①对于图2实验结果(注:T1、T2均大于300℃)
说法正确的是__________(填序号)。
a.向密闭容器中不断补充CO2,H2转化率增大
b.该反应在T1时的平衡常数比T2时小
c.温度为T1时,从反应开始到平衡,H2平均速率为![]()
d.平衡处于A点时密闭容器温度从T1变到T2,![]() 增大
增大
 ②300℃时,若充人1 mol CO2和
②300℃时,若充人1 mol CO2和
3 mol H2,从反应开始到平衡,测得CO2的转化率为75%。则平衡常数K为
(用最简分数表示)。
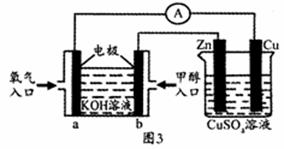
(5)将制备的甲醇(CH3OH)用于图3装置,其中b电极上发生反应的电极反应式为 ;
当铜片质量变化19.2 g时,a极上消耗的O2在标准状况下的体积为__ _L。
查看答案和解析>>
科目: 来源: 题型:
A、B、D、E为原子序数依次增大的短周期元素。A、B组成的气体甲能使湿润的红色石蕊试纸变蓝;A、D处于同一主族,E的最外层电子数等于其电子层数。
(1)B在元素周期表的位置是 ;四种元素的简单离子,半径最大的是 (填离子符号);D的单质在氧气中燃烧的产物电子式为 。
(2)B的一种氧化物BO2与水反应的化学方程式为
(3)甲和B的最高价氧化物的水化物反应生成乙。在0.1 mol·L-1乙溶液中,所含离子浓度由大到小的顺序是____ 。
(4)25℃时,E的最高价氧化物的水化物KSP=1.0×10-34,使含0.1 mol·L-1E离子的溶液开始产生沉淀的pH为 。
(5)已知298K时:Fe(s)+![]() O2(g)===FeO(s) △H=—272.0kJ•mol—1
O2(g)===FeO(s) △H=—272.0kJ•mol—1
2E(s)+![]() O2(g)===E2O3(s) △H=—1675.70kJ•mol—1
O2(g)===E2O3(s) △H=—1675.70kJ•mol—1
则E单质和FeO反应的热化学方程式为____ 。
查看答案和解析>>
科目: 来源: 题型:
右表是某铬酸(H2CrO4)溶液中离子浓度(mol•L-1)与pH的关系,下列说法不正确的是
A.铬酸一级电离方程式为H2CrO4 == H++HCrO4—
B.要得到CrO42—应控制溶液的pH>9
C.当电离达到平衡时,2v(正)(HCrO4—)= v(逆)(Cr2O72—)
D.该铬酸溶液的物质的量浓度约为1.00mol·L-1
| pH | c(CrO42—) | c(HCrO4—) | c(Cr2O72—) | c(H2CrO4) |
| 4 | 0.0003 | 0.1040 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0999 | 0.4370 | 0 |
| 7 | 0.2745 | 0.0860 | 0.3195 | 0 |
| 9 | 0.9960 | 0.0031 | 0.0004 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com