
科目: 来源: 题型:
在2 L的密闭容器中进行反应:4NH3(g)+3O2(g)===2N2(g)+6H2O。半分钟后N2的物质的量增加了0.6 mol。则半分钟内该反应的平均速率v(X)为
A.v(NH3)=0.02 mol·L-1·s-1 B.v(O2)=0.01 mol·L-1·s-1
C.v(N2)=0.02 mol·L-1·s-1 D.v(H2O)=0.02 mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.加入催化剂,能加快化学反应速率,同时提高了反应物的平衡转化率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.需要加热才能发生的反应一定是吸热反应
查看答案和解析>>
科目: 来源: 题型:
向0.5 L0.04mol·L-1H2SO4溶液中加入一定量的CuO粉末,充分反应后,把50 g铁丝放入该溶液中,至铁丝质量不再变化时,共收集到224 mL气体(标准状况)。求:(1)与硫酸反应的铁的物质的量。(2)CuO粉末的质量。
查看答案和解析>>
科目: 来源: 题型:
下面是印刷电路板的生产及其废液的处理的流程简图。请按要求填空:
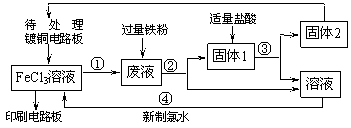
(1)镀铜电路版制成印刷电路版的离子方程式为 ;固体1的化学成
分是 (填化学式)。
(2)反应②的化学方程式为 ;要检验废液中是否含有Fe3+,所需的试剂是 (填化学式)溶液。
(3)反应④的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
海藻中富含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图。

(1)写出操作名称:操作① ,操作③ 。
(2)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件,3I2+6NaOH=5NaI+NaIO3+3H2O,Ks5u
酸性条件,5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+H2O。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的 (填仪器名称)中加入少量1mol·L-1 NaOH溶液;
②振荡至溶液的 色消失,静置、分层,则 (填“上”、“下”)层为CCl4;
③将含碘的碱溶液从仪器的 (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1 mol·L-1 H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(3)本实验中可以循环利用的物质是 。
查看答案和解析>>
科目: 来源: 题型:
某小组同学要配制100 mL 0.100 mol·L-1 Na2CO3溶液。下图是一些关键步骤和操作。
|
|
|
|
|
|
|
| A | B | C | D | E | F |
(1)配制过程的先后顺序为(用字母A~F填写) 。
(2)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、 。
(3)用Na2CO3·10H2O来配制溶液,若晶体已经部分失去结晶水,则所配得溶液的浓度会 (填“偏高”、“偏低”、“不变”)。
(4)步骤A通常称为洗涤,如果没有步骤A,则配得溶液的浓度将 (填“偏高”、“偏低”、“不变”);步骤F称为 ,如果俯视刻度线,配得溶液的浓度将 (填“偏高”、“偏低”、“不变”)。
(5)在步骤B之后,需 才进行下一步操作。
查看答案和解析>>
科目: 来源: 题型:
某学小组同学设计了以下三组实验验证某无色溶液中含有的离子:
 (1)溶液
(1)溶液
|
(2)溶液
|
|
(3)溶液
|
|
|
下列说法正确的是
A.该无色溶液有可能是明矾溶液
B.这三组实验中,只有(3)是严密合理的
C.步骤④的离子方程式为:Al3++3OH-=Al(OH)3↓
D.步骤⑥的化学方程式为:NaAlO2+H2O +CO2= Al(OH)3↓+NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com