
科目: 来源: 题型:
化学与生产和生活密切相关,下列说法正确的是
A.聚氯乙烯塑料薄膜可用作食品保鲜膜、一次性食品袋等
B.煤经过气化和液化等物理变化可转化为清洁燃料
C.淀粉、油脂和蛋白质都是高分子化合物
D.利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程
查看答案和解析>>
科目: 来源: 题型:
将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)(需要写出简单的求解步骤)
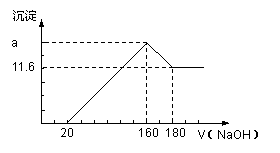 求:①合金中Mg的质量;
求:①合金中Mg的质量;
②所用HCl的物质的量浓度;
③a 的值.
查看答案和解析>>
科目: 来源: 题型:
利用图所示装置收集以下8种气体(图中烧瓶的位置不得变化)
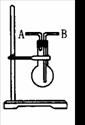 ①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
(1)若烧瓶是干燥的,则由B口进气收集的气体有________(写序号);
(2)若烧瓶充满水,可收集的气体有________,这时气体由________进入。
(3)若烧瓶是干燥的,则由A口进气,可收集的气体有________。
(4)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有________,这时气体由________口进入。
查看答案和解析>>
科目: 来源: 题型:
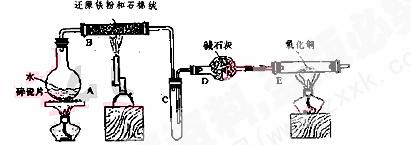 学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
(1)回答下列问题:所用铁粉中若有铝粉,欲除去混有的铝粉可以选用的试剂为
(填序号);
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D. FeCl3溶液
此步涉及反应的离子方程式为 ;经除杂后的铁粉进一步干燥后装入反应容器。
(2)反应发生后装置B中发生反应的化学方程式是_______________________________,D装置的作用___________________________;
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下:

①用离子方程式表示步骤I中通入Cl2的作用
(用单线桥表示电子转移的方向和数目);
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。
向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理 (填”合理”或”不合理”),若不合理,请你设计合理方案:
查看答案和解析>>
科目: 来源: 题型:
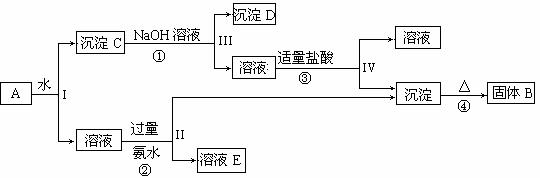 某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B ;C ;沉淀D ;溶液E 。
(3)写出①、②、③、④四个反应方程式(离子反应只写离子方程式)
① ;② ;
③ ;④ 。
查看答案和解析>>
科目: 来源: 题型:
过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+2CO=Na2CO3。
(1) 试分别写出Na2O2与SO2、SO3反应的化学方程式:
。 。
(2) 通过比较可知,当非金属元素处于 价时,其氧化物与过氧化钠反应有O2生成。
查看答案和解析>>
科目: 来源: 题型:
有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液,若将甲蒸发掉一半水分,在乙中通入少量的CO2,丙不变,然后分别向甲、乙、丙三瓶中加入同浓度的盐酸,完全反应后所需盐酸溶液的体积是 ( )
A.甲=乙=丙 B.丙>乙>甲 C.乙>甲=丙 D.甲=丙>乙
查看答案和解析>>
科目: 来源: 题型:
现有2mol·L-1的盐酸和硫酸溶液各100mL,分别加入等质量的铁粉,反应结束后,所生成的氢气的质量比为2∶3,则往酸中加入的铁粉的质量为
A.2.8g B.5.6g C.8.4g D.16.8g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com