
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 两份质量相等且组成完全相同的镁铝合金,一份投入足量的稀硫酸中,另一份投入足量的氢氧化钠溶液,生成氢气在标准状况下的体积与反应时间的关系如图.
两份质量相等且组成完全相同的镁铝合金,一份投入足量的稀硫酸中,另一份投入足量的氢氧化钠溶液,生成氢气在标准状况下的体积与反应时间的关系如图.查看答案和解析>>
科目: 来源: 题型:解答题
 硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:
硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]为浅绿色晶体,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小.实验室中常以废铁屑为原料来制备,其步骤如下:查看答案和解析>>
科目: 来源: 题型:解答题
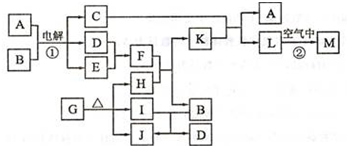
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 O2(g)△H2=242kJ?mol-1
O2(g)△H2=242kJ?mol-1 O2(g)=MgO(s)△H3=-602kJ?mol-1
O2(g)=MgO(s)△H3=-602kJ?mol-1
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com