
科目: 来源: 题型:单选题
如果长期大剂量食用铝含量超标的食品,成人可能导致老年痴呆,儿童会损害其智力发育.早在1989年世界卫生组织就把铝确定为食品污染源之一,加以控制使用.铝在下列应用中应该加以控制的是
①制铝合金 ②制电线 ③制炊具 ④明矾净水 ⑤明矾与苏打制食品膨松剂
⑥用氢氧化铝凝胶制胃舒平药片 ⑦银色漆颜色 ⑧易拉罐 ⑨包装糖果和小食品
查看答案和解析>>
科目: 来源: 题型:单选题
甘油跟新制的Cu(OH)2溶液混合时,能生成一种绛蓝色溶液,实验室据此法用来检验多羟基化合物。下列是关于甘油的叙述:
①甘油的水溶液呈弱酸性; ②甘油分子中的羟基具有极弱酸性;
③甘油能跟含氧酸发生酯化反应; ④甘油分子中羟基上的氢原子比一元醇分子中的羟基中氢原子活泼。
下列组合正确的是:
查看答案和解析>>
科目: 来源: 题型:解答题
有Ba(OH)2、NaHSO4、NaHCO3三种溶液,已知其中两种溶液的物质的量浓度相同,且分别为另一种溶液的物质的量浓度的2倍;若先将NaHSO4和NaHCO3溶液各 100mL混合反应后,再加入Ba(OH)2溶液100mL,充分反应后,将生成的白色沉淀滤出,测得滤液中只含一种NaOH溶质,其物质的量的浓度为0.9mol?L-1(不考虑溶液混和时引起溶液体积的变化),试回答:
(1)通过分析,判断原Ba(OH)2、NaHSO4、NaHCO3三种溶液中哪两种溶液的物质的量的浓度不可能相同?
(2)完成下表(可不填满,也可补充):
| c[Ba(OH)2]/mol?L-1 | c[NaHSO4]/mol?L-1 | c[NaHCO3]/mol?L-1 |
| ______ | ______ | ______ |
| ______ | ______ | ______ |
查看答案和解析>>
科目: 来源: 题型:解答题
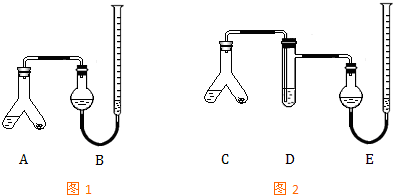 某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去.
某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
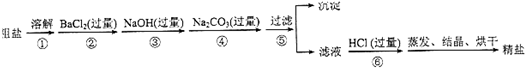
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com