
科目: 来源:2012-2013学年福建省三明一中高一上学期入学考试化学试卷(带解析) 题型:填空题
(4分)如图是甲、乙两种固体物质的溶解度曲线。
请回答:甲物质在45℃时的溶解度为 ;甲、乙两物质的溶解度相等的温度是 ℃;要使乙的不饱和溶液变为饱和溶液应 (填“升高”、“降低”)温度;常压下,CO2在水中的溶解度随温度的变化应类似于 (填:“甲”、“乙”)曲线。
查看答案和解析>>
科目: 来源:2011-2012学年吉林省吉林一中高一上学期期中考试化学试卷 题型:填空题
(6分)已知气体X2和气体Y2在一定条件下能化合生成气体C,并知C的化学式只有三种可能:XY、X2Y、X3Y。为确定C的化 学,某同学分别取同温同压下,体积都为V1的X2和Y2两种气体充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温后,再测出容器的容积(V2)。请填写下列结论与分析
学,某同学分别取同温同压下,体积都为V1的X2和Y2两种气体充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温后,再测出容器的容积(V2)。请填写下列结论与分析
(1)若实验结果(用V1、V2间关系来表示)是___________,则生成物C的化学式为XY,判断的依据是_____________________________________________________
(2)当生成物C的化学式为X2Y时,则实验结果是_____________,生成C的化学方程式为____________
查看答案和解析>>
科目: 来源:2011-2012学年黑龙江省哈师大附中高一10月份月考化学试卷 题型:填空题
气体化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10mLA气体能分解生成15mLO2和10mLF2(同温同压下),则A的化学式是 ,推断的依据是 和 。
查看答案和解析>>
科目: 来源:2012-2013学年福建省南安一中高一化学国庆节作业(一)(带解析) 题型:填空题
已知过氧化钠 投入水中能发生下列反应:2Na2O2+2H2O==4NaOH+O2↑。现将7.8g过氧化钠投入水中,充分反应后。计算:
(1)求生成的氢氧化钠的物质的量和氧气的体积。
(2)如反应后得到的溶液中Na+和水分子的个数比为1︰100,则开始时所用的水的质量是多少g?
查看答案和解析>>
科目: 来源:2012-2013学年福建省南安一中高一化学国庆节作业(一)(带解析) 题型:填空题
有一种氯化钠与氯化钾的混合物,它所含钾与钠的物质的量之比为3∶1,求:
(1)混合物中氯化钾的质 量分数。
(2)含1 mol Cl-的混合物的质量。
查看答案和解析>>
科目: 来源:2012-2013学年福建省南安一中高一化学国庆节作业(一)(带解析) 题型:填空题
Ⅰ.现有标准状况下的以下物质:
| A.11.2LO2 | B.6.8gNH3 | C.1.204×1024CH4 | D.0.5molCO2; |
查看答案和解析>>
科目: 来源:2012-2013学年福建省南安一中高一化学国庆节作业(一)(带解析) 题型:填空题
根据下列数据判断元素X的相对原子质量
(1)1.01*105Pa,273K时气态单质Xn的密度为d g/L,则X的相对原子质量为____________
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍,则X的相对原子质量_________________________
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为________________________
查看答案和解析>>
科目: 来源:2012-2013学年福建省南安一中高一化学国庆节作业(一)(带解析) 题型:填空题
一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液) + 3O2(气) = XO2(气) + 2YO2(气)冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是_ ______________。
②化合物XY2的摩尔质量是____________________。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_________和________。(写元素符号)
查看答案和解析>>
科目: 来源:2011-2012学年湖北省孝感高级中学高一上学期期末考试化学试卷(带解析) 题型:填空题
下图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积
的多少而变化的是________。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
查看答案和解析>>
科目: 来源:2013届上海市金山区高三上学期期末考试化学试卷(带解析) 题型:填空题
还原铁粉是冶金工业的重要原料,利用绿矾制备还原铁粉的工业流程如下: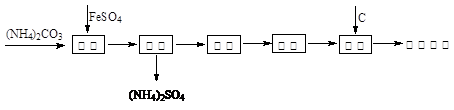
干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O被空气氧化为FeOOH,其化学方程式为 。
取干燥后的FeCO3样品12.49 g焙烧至600℃,质量变为8.00 g。所得产物用CO还原可得到Fe 6.16g。则600℃产物的可能组成是________________________________________。
根据以上数据可计算FeCO3样品中FeCO3与FeOOH的质量。FeCO3的质量为_________, FeOOH的质量为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com