
科目: 来源:2011届四川省南充高中高三第十三次月考(理综)化学部分 题型:实验题
洗车安全气囊是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的粉末进行实验。经组成分析,确定该粉末仅含Na、Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。
取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。单质乙在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另外一种单质。化合物丙置于空气中可转化为可溶性盐和一种气态单质。
请回答下列问题:
(1)甲的化学式为 ,丙的电子式为 。
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为 ;
将该碳酸氢盐溶于水配成溶液,则溶液中各离子浓度大小关系为: 。
(3)单质乙与红棕色粉末发生反应的化学方程式为 ,安全气囊中红棕色粉末的作用是 。
(4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是 。
| A.KCl | B.KNO3 | C.Na2S | D.CuO |
查看答案和解析>>
科目: 来源:2011届重庆市西南师大附中高三上学期期中考试(理综)化学部分 题型:实验题
下列是与硫元素相关的一系列实验:根据下图所示实验回答下列问题:
(1) 试管C口部的棉团上发生反应的离子方程式是 。
(2) 反应一段时间后,将B试管中的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3) 试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的离子方程式是 。
(4) 如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是 、 、 、 (要求填二种化合物和二种单质的化学式)。
(5) 取下C试管,试管中溶液浑浊,煮沸后,再加入Na2S溶液并加热,溶液变澄清,经测定溶液中主要存在一种摩尔质量为128g/mol的二价阴离子(反应①)。向该澄清液中加入氯水,溶液仍然澄清(反应②),加入氯化钡可得一种不溶于稀盐酸的白色沉淀,写出反应①和反应②的离子方程式 , 。
查看答案和解析>>
科目: 来源:2008年普通高等学校招生统一考试理综试题化学部分(四川卷) 题型:实验题
(08四川卷)某固体混合物可能含有MgCO3、Al2(SO4)3、Na2SO4Ba(NO3)2、AgNO3和CuSO4,将该混合物进行如下实验,根据所给实验现象完成表格(对于可能确定的物质在相应位置写化学式,暂不能确定的物质在相应位置填“无”)。
| 肯定存在的物质 | 肯定不存在的物质 | 理由 |
| | | |
| 肯定存在的物质 | 肯定不存在的物质 | 理由 |
| | | |
| 肯定存在的物质 | 肯定不存在的物质 | 理由 |
| | | |
查看答案和解析>>
科目: 来源:2012届湖南省衡阳八中高三第四次月考化学试卷 题型:计算题
(10分)已知高锰酸钾、二氧化锰在酸性条件下能将草酸钠(Na2C2O4)氧化:
MnO4—+C2O42—+H+―→Mn2++CO2↑+H2O(未配平);
MnO2+C2O42—+H+―→Mn2++CO2↑+H2O(未配平)。
为测定某软锰矿中二氧化锰的质量分数,准确称量1.20 g软锰矿样 品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题:
品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题:
(1)配平上述两个离子方程式:
___MnO+___C2O+___H+===___Mn2++___CO2↑+___H2O;
___MnO2+__C2O+___H+===___Mn 2++___CO2↑+__H2O。
2++___CO2↑+__H2O。
(2)欲求得软锰矿中二氧化锰的质量分数,还缺一个数据,这个数据是__________(填数据所代表的意义)。
(3)若该数据的数值为250,求该软锰矿中二氧化锰的质量分数(写出计算过程)。(4分)
查看答案和解析>>
科目: 来源:2012-2013学年河南省灵宝市第三高级中学高一上第三次质量检测化学(带解析) 题型:计算题
现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为多少?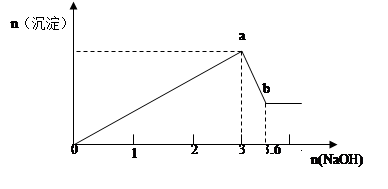
查看答案和解析>>
科目: 来源:2012-2013学年福建省莆田一中高一上学期期末考试化学试卷(带解析) 题型:计算题
某结晶水合物含有两种阳离子和一种阴离子。称取质量为1.96 g的该结晶水合物,配成溶液。加入足量Ba(OH)2溶液并加热该混合物,生成白色沉淀,随即沉淀变为灰绿色,最后变成红褐色,标况下产生224 mL能使湿润的红色石蕊试纸变蓝的气体;将沉淀过滤、洗涤并灼烧至恒重,得到固体粉末2.73 g;用足量稀盐酸处理上述粉末,洗涤和干燥后得到白色固体2.33 g。
(1)该结晶水合物含有的两种阳离子是__________和__________,阴离子是__________。写出产生能使湿润的红色石蕊试纸变蓝的气体的离子反应方程式: 。
(2)试通过计算确定该结晶水合物的化学式 。
查看答案和解析>>
科目: 来源:2012-2013学年吉林省长春二中高一上学期期末考试化学试卷(带解析) 题型:计算题
(16分) 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。则: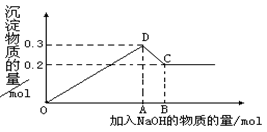
(1)写出代表各线段发生反应的离子方程式:
OD段 , _________________________________,
DC段 _。
(2)原溶液中Mg2+、Al3+物质的量浓度之比为 。
(3)图中C点表示当加入 mol NaOH时,Al3+已经转化为 Mg2+已经转化为 。
(4)图中线段OA∶AB= 。
查看答案和解析>>
科目: 来源:2013届湖北省孝感高中高三9月调研考试化学试卷(带解析) 题型:计算题
(12分)某混合溶液中可能含有的离子如下表所示:
| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH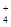 、Fe3+ 、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO 、AlO 、AlO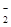 |

| Cl2的体积(标准状况) | 5.6 L | 11.2 L | 22.4 L |
| n (Cl-) | 2.5 mol | 3.0 mol | 4.0 mol |
| n (Br-) | 3.0 mol | 2.8 mol | 1.8 mol |
| n (I-) | x mol | 0 | 0 |
查看答案和解析>>
科目: 来源:2011年中国化学会第25届全国高中学生化学竞赛试卷 题型:计算题
(9分)固溶体BaInxCo1-xO3-δ是兼具电子导电性与离子导电性的功能材料,Co的氧化数随组成和制备条件而变化,In则保持+3价不变。为测定化合物BaIn0.55Co0.45O3-δ中Co的氧化数,确定化合物中的氧含量,进行了如下分析:称取0.2034 g样品,加入足量KI溶液和适量HCl溶液,与样品反应使其溶解。以淀粉为指示剂,用0.05000 mol/L Na2S2O3标准溶液滴定,消耗10.85 mL。
4-1 写出BaIn0.55Co0.45O3-δ与KI和HCl反应的离子方程式。
4-2 写出滴定反应的离子方程式。
4-3 计算BaIn0.55Co0.45O3-δ样品中Co的氧化数SCo和氧缺陷的量δ(保留到小数点后两位)。
查看答案和解析>>
科目: 来源:2012届河南省焦作十一中高三第一次月考化学试卷 题型:计算题
将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将5.405gX中Cr元素全部氧化成Cr2O72-,酸性的Cr2O72-可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O72-被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。(1)写出Cr2O72-与I-反应的离子方程式
(2)通过计算得出X的化学式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com