
科目: 来源:2011-2012学年河南省商丘市第二高级中学高一第一学期第二次月考化学试卷 题型:填空题
(10分)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为:
2KMnO4+16HCl(浓) ===2KCl+2MnCl2+5Cl2↑+8H2O
(1)请将上述化学方程式改写为离子方程式________________。
(2)浓盐酸在反应中显示出来的性质是________________(填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是 (填化学式),产生0.5molCl2,则转移的电子的物质的量为______mol。
(4).用双线桥法表示该反应的电子转移的方向和数目
查看答案和解析>>
科目: 来源:2011-2012学年贵州省凯里一中高一上学期期中考试化学试卷 题型:填空题
(10分)氧化还原反应在农业生产中和日常生活中有广泛的运用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 (填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中,维生素C所起的作用是 填“氧化作用”和“还原作用”)
(4)全世界每年有近1/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式: ,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用 方法(符合题意一种即可)防止铁生锈。
查看答案和解析>>
科目: 来源:2011-2012学年山东省临清三中高一第三次月考化学试卷 题型:填空题
在反应2KMnO4+16HCl 2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 ,氧化产物是 ;若有1mol KMnO4参加反应时,该反应转移电子的个数是 ;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为 mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。
2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 ,氧化产物是 ;若有1mol KMnO4参加反应时,该反应转移电子的个数是 ;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为 mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。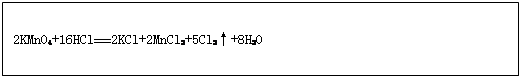
查看答案和解析>>
科目: 来源:2011-2012学年山东省临清三中高一第三次月考化学试卷 题型:填空题
(8分)阅读下列材料后,回答相应问题。
一个体重50Kg的健康人大约含铁2g,这2g铁在人体中不是以单质金属形式存在,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行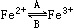 的相互转化,在A过程中,Fe2+做 剂,在B过程中,Fe3+做 剂。
的相互转化,在A过程中,Fe2+做 剂,在B过程中,Fe3+做 剂。
(2)“服用维生素C,可使食物中三价铁离子还原成二价铁离子。”这句话指出,维生素C在这一反应中做 _剂,具有 性。
(3)已知:氧化性Cl2> Br2> Fe3+, 还原性Fe2+>Br- >Cl-,则向0.2mol/L 1LFeBr2溶液中通入标准状况下氯气2.24L,被氧化的粒子是 ,此反应的离子方程式: 。
查看答案和解析>>
科目: 来源:2011-2012学年山西省大同一中高一上学期期中考试化学试卷 题型:填空题
(6分)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2↑+CO2↑。
(1) 其中被氧化的元素是 ,还原产物是 (填符号)。
(2) 当该反应生成6.72 L CO2(标况下)时,氧化剂一共得到 mol电子。
查看答案和解析>>
科目: 来源:2012届安徽省舒城中学高三第一学期期中考试化学试卷 题型:填空题
(14分,每空2分) 硫酸亚铁容易被氧化,而硫酸亚铁 铵晶体[(NH4)2SO4·FeSO4·6H2O]较稳定,常用于代替硫酸亚铁作还原剂。现以铁屑为主要原料制备硫酸亚铁铵晶体,其反应如下:Fe+H2SO4(稀)
铵晶体[(NH4)2SO4·FeSO4·6H2O]较稳定,常用于代替硫酸亚铁作还原剂。现以铁屑为主要原料制备硫酸亚铁铵晶体,其反应如下:Fe+H2SO4(稀) FeSO4+H2↑
FeSO4+(NH4)2SO4+6H2O (NH4)2SO4·FeSO4·6H2 O
O
步骤l:在盛有适量铁屑的锥形瓶里加入某种试剂除去油污,加热,充分反应后过滤、
洗涤、干燥、称量,铁屑质量为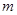 。
。
步骤2:将处理过的铁屑加入到一定量的稀H2SO4中,加热至50℃—80℃充分反应,
趁热过滤并用少量热水洗涤,滤液及洗涤液都转移至蒸发皿中。滤渣干燥后称重,剩余铁屑质量为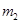 。
。
步骤3:准确称取所需质量的硫酸铵晶体加入“步骤2”的蒸发皿中,搅拌 使之溶解,
使之溶解,
缓缓加热一段时间,将其冷却结晶、过滤。用无水乙醇洗涤晶体并自然干燥,称量所 得晶体质量为
得晶体质量为 。
。
回答下列问题:
(1)能够用于除去铁屑表面油污的试剂是 (填字母)。
| A.纯碱溶液 | B.烧碱溶液 | C.明矾溶液 | D.稀硫酸 |
 (碱式硫酸铁),该反应的化学方程式为 。
(碱式硫酸铁),该反应的化学方程式为 。 H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。
H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。 晶体的产率为
晶体的产率为  。
。查看答案和解析>>
科目: 来源:2012届北京四中高三上学期期中测试化学试卷 题型:填空题
(7分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3—+4H++3e—→NO+2H2O KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的离子方程式:________________________________。
(2)反应中硝酸体现的性质有_________、__________。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________________mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: _______________________________________________________________________。
查看答案和解析>>
科目: 来源:2012届陕西省铁一中高三第二次模拟考试化学试卷 题型:填空题
(6分)2 g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075 mol/L KMnO4溶液处理,反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的 KMnO4恰好与350 mL 0.1 mol/L (NH4)2Fe(SO4)2溶液完全反应,反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5 Fe3+ +4H2O
(1) KMnO4溶液与混合物反应,消耗KMnO4的物质的量为 mol。
(2)欲配制500mL 0.1mol/L NH4+溶液,需称取 (NH4)2Fe(SO4)2·6H2O (M=392g/mol)的质量为 g。
(3)混合物中 Cu2S的质量分数为 。
查看答案和解析>>
科目: 来源:2012届陕西省铁一中高三第二次模拟考试化学试卷 题型:填空题
(6分)化合物BrFx与水按物质的量之比为3∶5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。(1)BrFx中,x= 。
(2)该反应的化学方程式是 。
(3)此反应中的氧化剂是_________和还原剂是_________。
查看答案和解析>>
科目: 来源:2011-2012学年山东省济宁市邹城二中高一上学期期中质量检测化学试卷 题型:填空题
(1)(8分)某反应体系中的物质有NaOH、Au2O3,Na2S4O6,Au2O,H2O,Na2S2O3。Au2O3为反应物,回答下列部题
| A.NaOH是(反应物、生成物) |
| B.Na2S4O6是(氧化剂、还原剂、氧化产物、还原产物) |
| C.氧化剂和还原剂的物质的量之比是 |
| D.0.25mol Au2O3发生反应,转移电子数是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com