
科目: 来源:2012-2013学年四川省资阳市高一上学期期末质量检测化学试卷(带解析) 题型:填空题
以下是依据一定的分类标准,对某些物质与水反应的情况进行分类的分类图。请根据你所学的知识,按要求填空:
(1)上述物质的分类方法是 ;
(2)根据物质与水反应的情况,分成A、B组的分类依据是 (选择字母填空,下同),由A组分成C、D组的依据是 (填字母)。
a.与水反应后溶液的酸碱性 b.与水反应的剧烈程度 c.是否发生氧化还原反应
(3)F组的物质是 (填化学式)。
(4)A组中的酸性氧化物与B组中的某物质反应可用作呼吸面具或潜水艇中氧气的来源,其反应方程式为 。
查看答案和解析>>
科目: 来源:2012-2013学年山东省威海市高二上学期期末考试化学试卷(带解析) 题型:填空题
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。某工厂使用还原沉淀法处理,该法的工艺流程为: 
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=12,则溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72-的浓度不变 b.Cr2O72-和CrO42-的浓度相同
c.2v(Cr2O72-)=v(CrO42-) d.溶液的颜色不变
(3)第②步反应中,还原剂为 ,该还原剂反应后生成 。
(4)电镀废液中Cr2O72-还可通过下列反应转化:
Cr2O72-(aq)+2Pb2+(aq)+H2O(l) 2 PbCrO4(s)+2H+(aq) ΔH< 0
2 PbCrO4(s)+2H+(aq) ΔH< 0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是 
查看答案和解析>>
科目: 来源:2012-2013学年河北省石家庄市第二实验中学高一上学期期中考化学卷(带解析) 题型:填空题
某一反应体系中,有反应物和生成物共六种物质,这六种物质是:Cl2、KMnO4、MnCl2、H2O、HCl(浓)、KCl,其中Cl2、H2O均为生成物。
(1)该反应中的氧化剂是 ,氧化产物为 。
(2)该反应中,氧化产物与还原产物的物质的量之比为 。
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中转移电子的数目为 NA(NA表示阿伏伽德罗常数的值),发生反应的KMnO4的质量为 g。
查看答案和解析>>
科目: 来源:2012-2013学年宁夏育才中学高一下学期期中考试化学试卷(带解析) 题型:填空题
根据氧化还原反应Fe + 2FeCl3 = 3FeCl2设计一个原电池装置。
(1)电解质溶液为
(2)负极材料 ,电极反应式
(3)正极材料 ,电极反应式
查看答案和解析>>
科目: 来源:2012-2013学年山东省威海市高一上学期期末考试化学试卷(带解析) 题型:填空题
一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+  Fe3+。在过程A中,Fe2+作 剂。
Fe3+。在过程A中,Fe2+作 剂。
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(3)某同学要检验Fe3+,向溶液中加入 (写化学式)溶液变成红色。要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是 (填字母)
a.铜粉 b.氯气 c.铁粉 d.KSCN溶液
查看答案和解析>>
科目: 来源:2012-2013学年浙江省某重点高中高一12月月考化学试卷(带解析) 题型:填空题
标出下列反应电子转移的方向和数目2KMnO4+16HCl(浓)==2KCl+2MnCl2+5Cl2↑+8H2O其中氧化剂的是 ,每生成1mol Cl2,电子转移了 mol。
查看答案和解析>>
科目: 来源:2013届江苏省南京学大教育专修学校高三4月月考化学试卷(带解析) 题型:填空题
某铜矿石含氧化铜、氧化亚铜、三氧化二铁和大量脉石(SiO2),现采用酸浸法从矿石中提取铜,其流程图如下:
已知: ①当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;②反萃取后的水层是硫酸铜溶液,Cu2+浓度约为50g/L。回答下列问题:
(1)矿石用稀硫酸浸出过程中氧化亚铜发生的反应为:Cu2O+2H+===Cu2++Cu+H2O;请写出该过程中发生的另一个氧化还原反应的离子方程式: 。
(2)写出用惰性电极电解水层的电解总反应方程式: 。
(3)循环中反萃取剂B的主要成分是 。
(4)某铜矿石样品中,若仅含氧化亚铜、三氧化二铁和脉石三种物质。取该矿石样品200.0g,用100mL1.0mol?L—1H2SO4溶液浸取后,还需加入10mL 1.0mol?L—1 Fe2(SO4)3溶液才能使铜全部浸出,浸取液经充分电解后可得到 6.4gCu。求铜矿石样品中氧化亚铜和氧化铁的质量分数?
查看答案和解析>>
科目: 来源:2013届上海市徐汇区高三上学期期末考试化学试卷(带解析) 题型:填空题
已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA族,+3价较稳定,Bi2O3为碱性氧化物,Bi3+的溶液为无色。取一定量硝酸酸化的Mn(NO3)2溶液依次进行下列实验,现象记录如下:
① 向其中加入适量的NaBiO3,溶液变为紫红色。② 继续滴加适量H2O2,紫红色褪去,并有气泡产生。③ 再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
写出实验①反应的离子方程式:______________________________________。
KMnO4、H2O2、PbO2氧化性由强到弱的顺序为____________________________。
向反应③得到的溶液中通入SO2气体,看到的现象是____________________________。
若实验②放出了336mL气体(标准状况),则反应①被氧化的Mn(NO3)2为________mol。
查看答案和解析>>
科目: 来源:2013届新疆乌鲁木齐地区高三第一次诊断性测验化学试卷(带解析) 题型:填空题
氧化还原滴定与酸碱中和滴定一样是化学实验室常用的定量测定方法。某氧化还 原滴定的反应体系中有反应物和生成物共六种,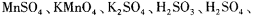
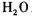 ,其中H2SO3的还原性最强,KMnO4的氧化性最强。对此反应体系:
,其中H2SO3的还原性最强,KMnO4的氧化性最强。对此反应体系:
(1) 被氧化的元素是_______;发生还原反应的过程是________→______。
(2) 请用这六种物质组织一个合理的化学反应,写出它的离子方程式:_______
(3) 反应中H2SO4是_______ (填编号)
A,氧化剂 B.氧化产物 C.生成物 D.反应物
(4) 当有20mL 0.1mol/L的氧化剂参加反应时,电子转移数目是_______ 。
(5) 用标准KMnO4溶液滴定H2SO3时,滴定终点时颜色变化是_______。
(6) 滴定过程中.下列图像所表示的关系正确的是_______(填编号)。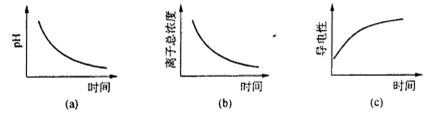
查看答案和解析>>
科目: 来源:2013届浙江省宁波一中2013届高三12月月考化学试卷(带解析) 题型:填空题
氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得: SiO2 + C + N2 Si3N4 + CO
Si3N4 + CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是 。
(3)分析反应可推测碳、氮气的氧化性:C N2(填“>”“<”“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com