
科目: 来源:2011-2012学年广东省揭阳第一中学高一第二次阶段考试化学试卷 题型:填空题
(3分)取两等份铝粉,第一份加入250 mL 2 mol·L-1的盐酸,第二份加入400 mL2mol·L-1的烧碱。若同温同压下放出气体体积之比为5:6,则加入的铝粉每份质量为 。
查看答案和解析>>
科目: 来源:2011-2012学年江西省南昌二中高一第二次月考化学试卷 题型:填空题
(10分) 将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如右图所示。当V1=140mL时,则金属粉末中n(Mg)= mol,V2= mL。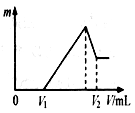
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入480 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:
(4)若滴加NaOH溶液致V2ml时,停止滴加NaOH溶液,开始往溶液中通入足量CO2,请写出发生反应的离子方程式——————————————————————-————。
查看答案和解析>>
科目: 来源:2011-2012学年北京市育园中学高二上学期期中考试化学(理)试卷 题型:填空题
(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,用化学方程式表示该反应的原理: 。
(2)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,用化学方程式表示该反应的原理: 。
(3)NaHCO3是制作糕点的常用疏松剂,写出NaHCO3受热分解的化学方程式:
(4)CH4与Cl2在光照条件下能生成CH3Cl,写出该反应的化学方程式:
(5)向硫酸亚铁溶液中滴入氢氧化钠溶液,生成的灰白色沉淀迅速变成灰绿色,最后变成红褐色,此过程中涉及的氧化还原反应的化学方程式为: 。
查看答案和解析>>
科目: 来源:2011-2012学年江西省安福中学高一第二次月考化学试卷 题型:填空题
(10分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化,据此回答下列问题: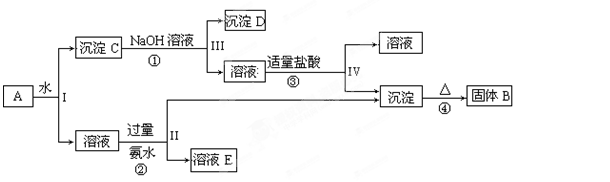
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2) 根据上述框图反应关系,写出下列B、D所含物质的化学式
根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B ;沉淀D 
(3)写出①、②、两个反应的离子方程式
①
②
查看答案和解析>>
科目: 来源:2011-2012学年山西省临汾一中高一12月月考化学试卷 题型:填空题
(16分)Ⅰ铝粉与某些金属氧化物组成的混合物叫铝热 剂,铝热剂在高温下发生的反应叫铝热反应。如:2Al+
剂,铝热剂在高温下发生的反应叫铝热反应。如:2Al+ Fe2O32Fe+Al2O3,反应发生时放出大量的热。仔细阅读上
Fe2O32Fe+Al2O3,反应发生时放出大量的热。仔细阅读上 述信息回答下列问题:
述信息回答下列问题:
(1)“铝热反应”属于四种基本反应类型中的________________反应。
(2)信息中的“某些”指__(填“比铝活泼的”“比铝不活泼的”或“任意”)。
(3)试写出铝粉与MnO2发生的铝热反应方程式
_____________________________________________________________。
(4)题给的铝热反应可用于野外焊接钢轨,试解释其基本原理________________________________________________________________。
II铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(5)铝制容器不能盛装NaOH溶液的原因(用离子方程式表示)
; (6)胃舒平是治疗胃酸(HCl)过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示): ;
(6)胃舒平是治疗胃酸(HCl)过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示): ;
碳酸氢钠也常用于治疗胃酸过多,写出反应的离子方程式:
;
(7)为完全沉淀氯化铝溶液中的铝元素,常加入过量的 ,反应的化学方程式: 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省梅州市曾宪梓中学高二12月月考化学试卷 题型:填空题
(12分)由短周期元素组成的A、B两种盐可发生变化,且B的焰色反应呈黄色(图中其他生成物未列出)
(1)无色溶液F中,一定含有的溶质的化学式为 。
(2)写出白色胶状沉淀C转化为无色溶液E的离子方程式________________________。
(3)A和B的混合物溶于水发生反应的离子方程式____________________________。
(4)B、E两溶液混合反应时,可观察到的现象是__________________________,写出其反应的 离子方程式_________________________________________________________。
离子方程式_________________________________________________________。
查看答案和解析>>
科目: 来源:2011-2012学年广东省广州市第五中学高一上学期期中考试化学试卷 题型:填空题
(16分 )镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015 t。从海水中(主要含含Na+,Cl—,Mg2+等离子)提取镁的工艺流程图如下:
)镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015 t。从海水中(主要含含Na+,Cl—,Mg2+等离子)提取镁的工艺流程图如下:
(1)A物质的化学式为 。操作1的名称为 。
(2)试写出向固体A中加入足量盐酸的离子方程式 。
(3)该反应的副产物主要有 等。
(4)若开始得到的固体A的质量为116g,不考虑物质的损失,则最后生成的Mg的物质的量为 mol。
查看答案和解析>>
科目: 来源:2011-2012学年广西武鸣高中高二上学期段考化学(理)试卷 题型:填空题
 (l2分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(l2分)铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应: 3CO(g)+
3CO(g)+ Fe2O3(s) ? 2Fe(s) +3CO2(g)
Fe2O3(s) ? 2Fe(s) +3CO2(g)
 该温度下,在2L盛有
该温度下,在2L盛有 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单 质铁11.2g。则10min内CO的平均反应速率为
质铁11.2g。则10min内CO的平均反应速率为  (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态: ① ②
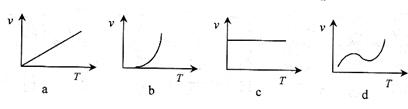
① ②  (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是 。
和温度(T)的关系示意图中与铝热反应最接近的是 。
 (4)写出氢氧化铝在水中发生电离的电离方程式:
(4)写出氢氧化铝在水中发生电离的电离方程式:  欲使上述体系中
欲使上述体系中 浓度增加,可加入的物质是 。
浓度增加,可加入的物质是 。
查看答案和解析>>
科目: 来源:2011-2012学年广西桂林十八中高二上学期期中考试化学(文)试卷 题型:填空题
(15分)在含 b mol AlCl3的溶液中加入含 a mol NaOH的溶液。
(1)、当a≤3b(即铝盐过量)时,生成Al(OH)3 沉淀的物质的量为 mol。
(2)、当a≥4b时,生成Al(OH)3 沉淀的物质的量为 mol。
(3)、当3<a/b<4时,先有沉淀生成,后又有部分沉淀溶解,此时Al(OH)3的物质的量为 mol。
(4)、请写出AlCl3与NaOH溶液反应时三个有关的离子方程式或化学方程式:
①:
②:
③:
查看答案和解析>>
科目: 来源:2011-2012学年浙江省瑞安中学高二上学期期中考试化学(文)试卷 题型:填空题
(6分)右图是某厂生产的一盒氢氧化铝片标签的部分内容,据此回答以下问题:
| 氢氧化铝片 Aluminium Hydroxide Tablets |
| 【主要成分】糖衣、碳酸镁、氢氧化铝、淀粉 |
| 【适应症】能缓解胃酸过多 |
| 【用法用量】成人:口服,一次0.6~0.9g(一次2~3片),一日3次,餐前1小时服。 |
| 【详细用法】见说明书 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com