
科目: 来源:2011-2012学年重庆市杨家坪中学高二上学期期中考试化学试卷 题型:计算题
已知Fe2O3在高炉中有下列反应:Fe2O3+CO=2FeO+CO2反应形成的固体混合物(Fe2O3、FeO)中,元素铁与氧的质量比用m (Fe):m (O)表示。
⑴ 上述固体混合物中,m (Fe):m (O)不可能是 (选填A、B、C)
上述固体混合物中,m (Fe):m (O)不可能是 (选填A、B、C)
A.21:9 B.21:7.5 C.21:6
⑵若m (Fe):m (O)=21:8,计算Fe2O3被还原的百分率。
查看答案和解析>>
科目: 来源:2012届山西省太原市高三第一学段测评考试化学试卷 题型:计算题
(8分)某工厂用FeC13溶液腐蚀镀有铜的绝缘板生产印刷电路。
(1)用离子方程式表示其化学原理 。
某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL。废液,向其中加入0.64 g金属铜,金属铜全部溶解;又取50.00 mL废液,向其中加入足量AgNO3溶液,析出沉淀43.05 g。请回答以下问题:
(2)该厂生产后废液中所含金属阳离子有
(3)该厂原来使用的FeCl3溶液的物质的量浓度为 。(设反应前后溶液的体积无变化);
(4)若向500.00 mL废液中加入足量的稀硝酸,在
标准状况下生成NO气体4.48 L,则原废液中各
金属阳离子的物质的量浓度之比为 。(离
子与比值一一对应)。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省余姚中学高一上学期期中化学(理)试卷(化学实验班) 题型:计算题
某工厂化验室为测定某黄铁矿(主要成分是FeS2)的纯度,取1.00 g矿石样品(所含杂质不挥发且不与氧气反应),在氧气流中充分灼烧,完全反应后,冷却,称量固体残留物,质量为0.75g。
(1)该黄铁矿中FeS2的质量分数为多少?
(2)该工厂用这种黄铁矿制硫酸,在FeS2燃烧过程中损失2%,由SO2氧化成SO3时,SO2的利用率为80%,吸收塔中SO3完全吸收。若煅烧10 .0t上述黄铁矿,则可制得98%的硫酸多少吨?
查看答案和解析>>
科目: 来源:2011-2012年湖南省师大附中高一上学期期中考试化学试卷 题型:计算题
(6分)将足量铁投入到200mLH2SO4和CuSO4的混和溶液中,充分反应后,产生H21.12L(标准状况),铁块的质量减轻了1.2g。求原溶液中c(H2SO4)及c(CuSO4)。(假设反应前后溶液的体积不变)
查看答案和解析>>
科目: 来源:2011--2012学年湖北省部分重点中学高三第一次联考试题化学试卷 题型:计算题
(6分)硫酸亚铁可与等物质的量的硫酸铵生成硫酸亚铁铵:(NH4)2SO4·FeSO4·6H2O,商品名称为莫尔盐,是一种复盐。一般亚铁盐在空气中易被氧气氧化,形成复盐后就比较稳定。与其他复盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,且几乎不溶于乙醇,利用这一性质可以制取硫酸亚铁铵晶体。三种盐的溶解度(单位为g/l00gH2O)见下表: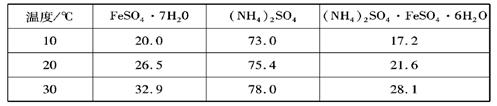
实验用品:10% Na2CO3溶液、Fe屑、3mol/LH2SO 4、( NH4)2SO4、蒸馏水、无水乙醇。
4、( NH4)2SO4、蒸馏水、无水乙醇。
实验步骤流程图: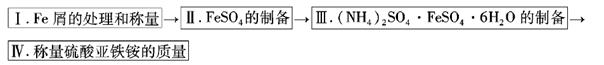
请完成以下实验记录:
(1)步骤I中处理铁屑所用试剂为________________,经处理后的干燥铁屑质量记为m1;
(2)将称量好的Fe屑放入锥形瓶中,加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全)。趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中。将滤纸上的固体常温干燥后称重,记为m2;
(3)称取一定质量的(NH4)2SO4,加入______ g(用含m1和m2的代数式表示,要求化简,下同。)水配制成室温下( 20℃)的饱和溶液,并将其加入到上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止。放置冷却,得到硫酸亚铁铵的晶体,过滤后用________________洗涤晶体。
(4)称量生成的硫酸亚铁铵的质量,理论上为________________g。
查看答案和解析>>
科目: 来源:2011-2012学年甘肃省张掖中学高二上学期期中考试化学(文)试卷 题型:计算题
把2.0 mol/L CuSO4溶液和1.0 mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。计算:
(1)混合溶液中CuSO4的物质的量浓度;
(2)向溶液中加入足量的铁粉,经足够长的时间后,铁粉有剩余。此时溶液中的Fe2+的物质的量浓度。
查看答案和解析>>
科目: 来源:2012届新疆乌鲁木齐一中高三第二次月考化学试卷 题型:计算题
现有铁和铜组成的合金共a mol,其中铜的物质的量分数为x。将此合金研成粉末状后全部投入含b mol硝酸的稀溶液中,微热使其充分反应,硝酸的还原产物只有NO。
(1)用粒子符号填写下列空白(列举出全部可能出现的情况):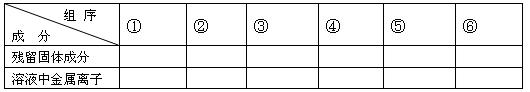
(2)当溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围为(用a、x表示)
(3)当x=0.5时,溶液中Fe3+和 Fe2+的物质的量相等,在标准状况下共生成672毫升NO气体,求a和b的值。
查看答案和解析>>
科目: 来源:2012届四川省南充高中高三上学期第二次月考化学试卷 题型:计算题
(8分)黄铜矿的主要成分X是由Cu、Fe、S三种元素组成的复盐,其中Cu、Fe两种元素的质量比为8∶7;将m g X粉末全部溶于200 mL的浓HNO3,反应后的溶液加水稀至 2.12 L时测得其pH=0;将稀释后的溶液分为两等份,向其中一份溶液中滴加浓度为6. 05 mol/L的NaOH溶液,向另一份溶液中滴加0.600 mol/LBa(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶
05 mol/L的NaOH溶液,向另一份溶液中滴加0.600 mol/LBa(NO3)2溶液,两溶液中均生成沉淀,且沉淀的质量随所加溶 液的体积变化如下图所示:
液的体积变化如下图所示: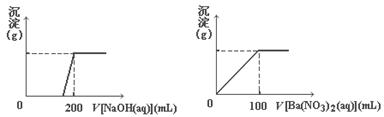
(1)请通过计算确定:m=________。
(2)X的摩尔质量为368 g/mol,则X的化学式为________________。
(3)将一定质量的Fe、Cu的混合物平均分成四等份,每份13.2 g,分别加入同浓度的稀硝酸 ,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO):
,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO):
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
查看答案和解析>>
科目: 来源:2012届江苏省致远中学高三第一次教学质量检测化学试卷 题型:计算题
(10分)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3 =" 2" CuCl ↓+ 3 Na2SO4 + CO2↑
⑴ CuCl制备过程中需要配制质量分数为20.0% 的CuSO4溶液,试计算配制该溶液所需的CuSO4·5H2O与H2 O的质量之比。
O的质量之比。
⑵准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:
Fe 3++CuCl=Fe 2++Cu2++Cl-,Ce4+ + Fe 2+ = Fe 3+ + Ce3+
通过计算说明上述样品中CuCl的质量分数是否符合标准。
查看答案和解析>>
科目: 来源:2012届高三上学期单元测试(6)化学试卷(新人教版) 题型:计算题
(9分)现有一种铜和氧化亚铁的混合物样品。为测定该样品中氧化亚铁的含量,某学生取20.0g此样品置于烧瓶中,分四次加入密度为1.22g/cm3的硫酸并做相关记录。有关数据记录如下表:
| 加硫酸的序号 | 每次加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 16.0 |
| 2 | 20.0 | 12.0 |
| 3 | 20.0 | 8.0 |
| 4 | 20.0 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com