
科目: 来源:2010年高考化学试题分项专题十四 化学计算 题型:填空题
硫——碘循环分解水制氢主要涉及以下反应
I SO2+2H2O+I2=H2SO4+2HI
II 2HI H2+I2
H2+I2
III 2H2SO4=2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是__________
a.反应III易在常温下进行 b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O d.循环过程中产生1mol O2的同时产生1 molH2
(2)一定温度下,向1L密闭容器中加入1 molHI(g),发生反应II,H2物质的量随时间的变化如图所示。
0—2min已见分晓的平均反应速率v(HI)=_____________,该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=__________。
2HI(g)的平衡常数K=__________。
相同温度下,若开始加入2HI(g)的物质的量是原来的2倍,则_____是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制H2,反应时候溶液中水的电离平衡________移动(填“向左”或“向右”或“不”);若加入少量下列试剂中的__________,产生H2的速率将增大。
| A.NaNO3 | B.CuSO4 | C.Na2SO4 | D.NaHSO3 |
 。
。查看答案和解析>>
科目: 来源:2010年吉林一中高三冲刺(理科综合)化学部分 题型:填空题
TiO2在工业生产和日常生活中有重要用途。
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答: (填“需要”或“不需要”)。
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式。
答: 。
II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti(同时产生O2):将处理过的TiO2作阴极,石墨为阳极,熔融CaCl2为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为___________________________________。
(4)电解过程中需定期向电解槽池中加入碳块的原因是______________________。
“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti。因下述反应难于发生:
TiO2 (s)+2Cl2 (g) TiCl4(l)+O2 (g) ΔH=+151 kJ·mol-1
TiCl4(l)+O2 (g) ΔH=+151 kJ·mol-1
所以不能直接由TiO2 和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(5)已知:C(s)+O2 (g) = CO2 (g) ΔH=-394 kJ·mol-1。请填空:
TiO2 (s)+C (s)+2Cl2 (g) = TiCl4 (l)+CO2 (g) ΔH= ______________
(6)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因。
答:____________________________________________。
查看答案和解析>>
科目: 来源:2010年四川省成都石室中学高三高考模拟考试(理科综合)化学部分 题型:填空题
(19分)已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC,K只知含有CO或CO2中的一种或两种。它们关系如图: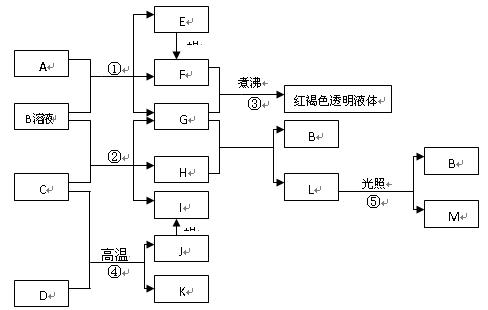
(1)写出下列物质的化学式: A D
(2)写出下列反应的化学方程式:
②
⑤
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用 方法(填序号)
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为
当反应转移1mol电子时,负极质量增加 g。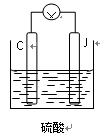
查看答案和解析>>
科目: 来源:2010年河南省郑州外国语学校全真模拟(二)(理科综合)化学部分 题型:填空题
(15分)
(1)下列事实中,能证明亚硫酸的酸性强于氢硫酸的是 (填字母)。
a.亚硫酸受热时易分解
b.相同条件下,等浓度的亚硫酸溶液导电能力强于氢硫酸
c.亚硫酸溶液可使品红溶液褪色,而氢硫酸不能
d.常温下,浓度均为0.k^s*5#u1mol/L的H2SO3溶液和H2S溶液的pH分别是2.k^s*5#u1和4.k^s*5#u5
(2)工业上除去高压锅用水中溶解的氧气常用的试剂有Na2SO3和N2H4(肼)。
①已知16g液态的肼与氧气反应得到氮气和液态水时,放热354.k^s*5#u87kJ,该反应的热化学方程式是 。
②除去等质量的O2,所耗Na2SO3和N2H4的质量比是 (填最简整数比)。
(3)向Na2SO3和Na2S的混合溶液中加入稀盐酸,溶液中会产生大量淡黄色沉淀。则该反应中氧化剂和还原剂的物质的量之比是 。
(4)已知Na2SO3在高温下发生分解,得到两种产物。某同学称取25.k^s*5#u2g纯净的Na2SO3·7H2O晶体在高温下隔绝空气加热至恒重,冷却后称得固体为12.k^s*5#u6g,将其完全溶于水配成1L溶液,并测溶液的pH。
①Na2SO3高温分解的化学方程式是 。
②测得溶液的pH大于0.k^s*5#u025mol/LNa2SO3溶液的pH,试解释原因(结合离子方程式说明) 。
查看答案和解析>>
科目: 来源:2010年浙江省浙东北三校高一第二学期期中联考化学试题 题型:填空题
(10分)A、B、C、D 4种元素,其中A、B、C为短周期元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B元素的名称 ;B在周期表中的位置第 周期,第 族;
(2)A、B形成的化合物的电子式 ;
(3)C的元素符号 ,C的最高价氧化物的化学式 ;
(4)D的最高价氧化物对应的水化物的化学式 。
查看答案和解析>>
科目: 来源:2010年浙江省浙东北三校高一第二学期期中联考化学试题 题型:填空题
(6分)有X、Y、Z三种主族元素形成的3种离子X(n+1)+,Y m-,Z m+,已知m > n,X(n+1)+比Z m+多一个电子层,Z与Y同周期,则进行下列推断:
(1)X、Y、Z三种原子的原子半径由大到小的顺序是 > > 。
(2)X(n+1)+、Y m-、Z m+三种离子的半径由大到小的顺序是 > > 。
(3)三种元素最高价氧化物对应水化物碱性依次减弱,酸性依次增强的顺序
是 (填X、Y、Z)。
查看答案和解析>>
科目: 来源:2010年福建省厦门第一中学高一第二学期期中考试化学试题 题型:填空题
(5分)已知溴单质的 氧化性介于氯和碘之间,利用这一性质解决下面问题
氧化性介于氯和碘之间,利用这一性质解决下面问题
(1)下列可以氧化Br-微粒是 (填序号)。
A.I2 B. I- C.Cl2 D.Cl-
(2)把滤纸用淀粉和碘化钾的溶液浸泡、晾干后可获得实验常用的淀粉碘化钾试纸。这种试纸润湿后遇氯气变化的现象是 ,用化学方程式解释该现象: 。
(3)下列试剂不能把NaCl和KI两种无色溶液区别开的是 (填序号)。
A. 氯水 B. 溴水 C. 淀粉溶液
查看答案和解析>>
科目: 来源:广东省广州市番禺区2010届高三第四次统测理综化学试题 题型:填空题
锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4 = ZnS↓+BaSO4↓。以下是工业生产流程。请回答有关问题:
Ⅰ.ZnSO4溶液的制备与提纯
有关资料:已知Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2;
菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等。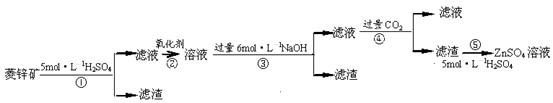 (1)②中使用的氧化剂最好是下列的 (填序号),理由是 。
(1)②中使用的氧化剂最好是下列的 (填序号),理由是 。
| A.Cl2 | B.H2O2 | C.KMnO4 | D.浓HNO3 |
 有关数据: Ba(s)+S(s)+2O2(g)=BaSO4(s);△H = —1473.2 kJ?mol-1
有关数据: Ba(s)+S(s)+2O2(g)=BaSO4(s);△H = —1473.2 kJ?mol-1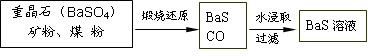
查看答案和解析>>
科目: 来源:2010年江苏省徐州市高三第三次调研考试(化学试题) 题型:填空题
近年,我国在航天事业上取得了令世界瞩目的成就,神舟飞船多次被长征系
列火箭送入太空。
(1)长征二号捆绑式火箭推进剂以联氨(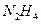 )作为燃料,
)作为燃料, 作为推进剂。
作为推进剂。
① 的主要作用是助燃,但其在工作时会产生红棕色气体
的主要作用是助燃,但其在工作时会产生红棕色气体 ,对环境会造
,对环境会造
成污染,为避免污染可使用下列 (填字母)代替之。
| A.液态氨 | B. | C.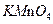 | D.液态氧 |
 和次氯酸钠反应可以制取联氨(产物中
和次氯酸钠反应可以制取联氨(产物中
 、
、 和 ;装置Ⅱ中
和 ;装置Ⅱ中 的来源,若宇航员每天消耗35mol
的来源,若宇航员每天消耗35mol ,每天呼出
,每天呼出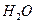 ,则呼出的气体中含
,则呼出的气体中含 mol.
mol.查看答案和解析>>
科目: 来源:2010年重庆市南开中学高三考前第一次模拟(理综)化学部分 题型:填空题
(16分)
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y.已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题: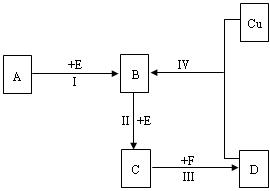
(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为 。
②反应Ⅰ的化学方程式为 。
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式 。
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol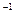 ,则:
,则:
①反应Ⅳ的溶液加热蒸干所得的晶体属于 晶体(填“离子”、“分子”、“原子”).
②反应I的化学方程式为 。
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com