
科目: 来源:2010年湖南省衡阳八中高三上学期第二次月考化学试题 题型:计算题
(2分)相同质量的钠、镁、铝与过量的稀硫酸反应,在状况下产生氢气的质量比是 ,若过量的相同质量的钠、镁、铝与相同质量分数,相同质量的稀硫酸溶液反应,产生氢气最多的是 。
查看答案和解析>>
科目: 来源:2010年安丘中学高二暑期练习化学卷(一) 题型:计算题
(8分)氯化钙是用途广泛的化学试剂,可作干燥剂、冷冻剂、防冻剂等。为了测定某氯化钙样品中钙的含量,进行如下实验:
①准确称取氯化钙样品0.2312g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35mL0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
②过滤并洗涤①所得沉淀。
③加入足量的10% H2SO4和适量的蒸馏水,②中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热加入0.05mol/L KMnO4溶液16mL,恰好完全反应。
回答下列问题:
(1)配平: MnO4-+ H2C2O4+ H+― Mn2++ CO2↑+ H2O
(2)0.05mol·L-1KMnO4标准溶液应置于 (选填“酸式”或“碱式”)滴定管中;判断滴定终点的现象为 。
(3)计算该氯化钙样品中钙元素的质量分数(精确到0.01%)。
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题十四 化学计算 题型:计算题
Na2SO3·7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂。Na2SO3在30℃时的溶解度为35.5g/100gH2O。
1)计算30℃时Na2SO3饱和溶液中Na2SO3的质量分数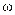 。(保留2位小数)
。(保留2位小数)
2)计算30℃时271g Na2SO3饱和溶液中水的质量。
3)将30℃的Na2SO3饱和溶液271g冷却到10℃,析出Na2SO3·7H2O晶体79.5g。计算10℃时Na2SO3在水中的溶解度。
查看答案和解析>>
科目: 来源:炎德?英才大联考三湘名校2010届高三月考试卷(一) 题型:计算题
(每空3分,共9分)在50mL amol/L的硝酸溶液中,加入6.4gCu,全部溶解,假设 硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO
硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO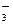 )=3mol/L,
)=3mol/L,
(1)稀释后溶液c(H+)=_____ mol
mol /L。
/L。
(2)若a=9,则生成的气体中NO2的物质的量为____mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO3+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
若将上述的NO2和NO的混合气体通入1mol/L的NaOH恰好被吸收,则NaOH溶液的体积为______mL。
查看答案和解析>>
科目: 来源:东北师大附中2009—2010学年高一上学期期末(化学)试题 题型:计算题
(6分)在隔绝空气的条件下,某同学将一块被氧化钠覆盖的钠块用一张无保护膜并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待反应完全后,在容器中收集到1.12L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内溶液的总体积为2.0L,溶液中NaOH的浓度为0.050mol·L-1(忽略溶解的氢气的量)。试通过计算确定该钠块中钠元素的质量分数。
查看答案和解析>>
科目: 来源:2012-2013学年广东省汕头市金山中学高一下学期期末考试化学试卷(带解析) 题型:填空题
按要求完成以下方程式:
(1)磁性氧化铁溶于盐酸的化学方程式:_________________________________________。
(2)氯化铁溶液中通入SO2气体的离子方程式:_______________ ____________________。
(3)偏铝酸钠溶液中通入过量CO2的离子方程式:_________________________________。
(4)碳单质和浓硝酸反应的化学方程式:_________________________________________。
查看答案和解析>>
科目: 来源:2012-2013学年四川成都棠湖中学外语实验学校高二5月月考化学卷(带解析) 题型:填空题
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。(已知:碳酸不能溶解Al(OH)3沉淀)
(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3 b.结合质子的能力:CO> AlO2->HCO3-
c.稳定性:H2O>CH4>SiH4 d.离子半径:O2-<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是
通过 现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,主要两个目的是 , ;
若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg ,理论上至少需要1 mol L-1 HNO3的体积为 L。
查看答案和解析>>
科目: 来源:2012-2013学年吉林省吉林一中高二4月月考化学试卷(带解析) 题型:填空题
含有较多可溶性______________化合物的水叫硬水,不含或含较少可溶性______________化合物的水叫软水.区别硬水和软水的试剂是______________,现象是______________,长期盛硬水的容器易______________.
查看答案和解析>>
科目: 来源:2012-2013学年湖南省怀化市高一上学期期末考试化学试卷(带解析) 题型:填空题
有下列四种物质:①SiO2 ②HF ③NaHCO3 ④Na2O2 按要求填空(填序号):
(1)常用来作为呼吸面具或潜水艇中供氧剂的是 。
(2)可以在玻璃上刻字、雕刻花纹的是 。
(3)可以作为食用碱,也是焙制糕点发酵粉的主要成份的是 。
(4)由它制成的光导纤维,抗干扰性能好,通信质量高,并且能防窃听,是当前信息社会必不可少的高技术材料,它是 。
查看答案和解析>>
科目: 来源:2012-2013学年山东省济宁市任城一中高一3月质量检测化学试卷(带解析) 题型:填空题
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1) 写出C的化学式 ,H的电子式 。
(2) B与氢氧化钠溶液反应的化学方程式为: 。
(3) G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为 ,当生成2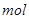 二氧化氯时,转移电子
二氧化氯时,转移电子 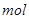 。
。
(4) 溶液F在空气中长期放置生成H的化学反应方程式为:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com