
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 (1)按要求完成下列表格:
(1)按要求完成下列表格:| 实验要求 | 化学试剂(写化学式) | 主要操作 |
| 除去NO气体中混有的NO2 | ______ | ______ |
| 除去SiO2固体中混有的Al2O3 | ______ | ______ |
| 除去Na2CO3溶液中的NaHCO3 | ______ | - |
| 除去NaCl溶液中混有的I2水溶液 | ______ | ______ |
查看答案和解析>>
科目: 来源: 题型:单选题
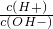 =10-12溶液中:Na+、K+、CO32-、NO3-
=10-12溶液中:Na+、K+、CO32-、NO3-查看答案和解析>>
科目: 来源: 题型:解答题
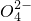 )≤1.0×10-5 mol?L-1,应保持溶液中c(Ba2+ )≥______mol?L-1.
)≤1.0×10-5 mol?L-1,应保持溶液中c(Ba2+ )≥______mol?L-1.查看答案和解析>>
科目: 来源: 题型:解答题
 ?
?| 实验现象 | 原因 | |
| 溶液最初从紫色逐渐变为______色 | 氯气与水反应生成的H+使石蕊变色 | |
| 随后溶液逐渐变为无色 | ______色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com