
科目: 来源:2010—2011学年海南省嘉积中学高一下学期质量检测(一)化学试卷 题型:单选题
原子序数大于4的主族元素X、Y的离子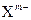 、
、 核外电子层结构相同,则关于X、Y两元素的叙述正确的是
核外电子层结构相同,则关于X、Y两元素的叙述正确的是
| A.X的原子序数小于Y的原子序数 |
| B.X、Y的核电荷数之差是(m-n) |
| C.Y元素的族序数与X元素的族序数之差是8-(m+n) |
| D.X和Y处于同一周期 |
查看答案和解析>>
科目: 来源:2010—2011学年浙江省杭州市西湖高级中学高一4月月考化学试卷 题型:单选题
据报道,元素钬有一种放射性核素 可有效治疗肝癌。该核素原子核内的中子数为
可有效治疗肝癌。该核素原子核内的中子数为
| A.67 | B.99 | C.166 | D.233 |
查看答案和解析>>
科目: 来源:2011届河南省普通高中毕业班高考适应性测试试卷(理综)化学部分 题型:单选题
关于反应:RO3—+( )+6H+ 3R2↑+3H2O的下列说法中,正确的是 ( )
| A.R一定是周期表中的第VA族元素 |
| B.RO3—中的R元素在该反应中被氧化 |
| C.R是同周期元素中原子半径最大的元素 |
| D.上式括号中所填物质在反应中作还原剂 |
查看答案和解析>>
科目: 来源:2010—2011学年福建省厦门市杏南中学高一3月月考化学试卷 题型:单选题
元素X原子的最外层有3个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物的化学式可能是(元素X、Y都为主族元素)
| A.XY2 | B.X2Y3 | C.X3Y2 | D.X2Y |
查看答案和解析>>
科目: 来源:2010—2011学年福建省厦门市杏南中学高一3月月考化学试卷 题型:单选题
下列各组元素性质或原子结构递变情况错误的是
| A.Li、Be、B原子最外层电子数依次增多 | B.P、S、Cl元素最高正化合价依次升高 |
| C.N、O、F原子半径依次增大 | D.Li、Na、K的电子层数依次增多 |
查看答案和解析>>
科目: 来源:2010—2011学年福建省厦门市杏南中学高一3月月考化学试卷 题型:单选题
某主族元素最外层只有1个电子,则该元素一定是:
| A.ⅠA族元素 | B.第ⅦA元素 | C.第三周期元素 | D.金属元素 |
查看答案和解析>>
科目: 来源:2010—2011学年浙江省余姚中学高一下学期第一次质量检测化学试卷 题型:单选题
下列排列顺序正确的是
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④物质的熔点 :石英>食盐>冰
:石英>食盐>冰
| A.①③ | B.②④ | C.①④ | D.②③ |
查看答案和解析>>
科目: 来源:2011届浙江省绍兴一中高三下学期回头考试(理综)化学部分 题型:单选题
下列推断合理的是( )
A.在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;在高温下,Na2CO3+SiO2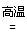 Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3 Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3 |
| B.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则 c[(NH4)2SO4]>c[(NH4  )2CO3] >c[(NH4)2Fe(SO4)2] )2CO3] >c[(NH4)2Fe(SO4)2] |
| C.向1L0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中 2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
| D.在海带中提取碘的实验中既可以用四氯化碳作萃取剂也可以用酒精作萃取剂 |
查看答案和解析>>
科目: 来源:2011届浙江省绍兴一中高三下学期回头考试(理综)化学部分 题型:单选题
A、B、C、D、E是五种短周期元素。A、B、C位于同一周期的相邻位置,它们分别与D形成10电子分子,且A、C原子序数之比为3:4。E原子从内到外各电子层的电子数之比为1:4:2。则下列叙述或分析正确的是( )
A.晶体熔点:AC2﹤EC2,主要因为相对分子质量:AC2﹤EC2
B.氢化物沸点:A﹤C, 主要因为相对分子质量:A﹤C
C.气态氢化物稳定性:E﹤A﹤B﹤C
D.A、B、C、D四种元素形成的化合物一定属于无机盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com