
科目: 来源: 题型:单选题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 过量铁加入稀硝酸中,充分反应后,滴加KSCN溶液 | 溶液呈红色 | Fe被氧化成Fe3+ |
| B | 将某气体通入品红溶液中 | 品红褪色 | 气体一定是SO2 |
| C | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝色 | 原溶液中没有NH4+ |
| D | 向某溶液中滴加氯水和四氯化碳,震荡、静置 | 下层溶液呈紫色 | 原溶液中一定有I- |
查看答案和解析>>
科目: 来源: 题型:单选题
 Fe2O3+3H2O
Fe2O3+3H2O查看答案和解析>>
科目: 来源: 题型:解答题
 某校学生在实验室中设计了如下装置,模拟侯德榜制碱法,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,再将碳酸氢钠晶体加热分解而制得碳酸钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
某校学生在实验室中设计了如下装置,模拟侯德榜制碱法,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,再将碳酸氢钠晶体加热分解而制得碳酸钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目: 来源: 题型:单选题
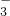 +H2O?H2CO3+OH-
+H2O?H2CO3+OH-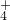 +OH-
+OH-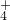
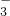 +OH-=H2O+CO
+OH-=H2O+CO
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
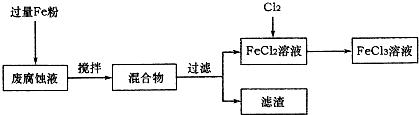

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com