
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
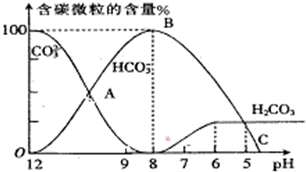 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题: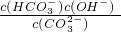 =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______. H++HA- HA-
H++HA- HA- H++A2-
H++A2-查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
 H2CO3+2OH-
H2CO3+2OH-查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
现有下列十种物质:①Cu(OH)2 ②干冰 ③Cu ④纯碱 ⑤BaCl2 ⑥Ca(OH)2 ⑦稀硝酸 ⑧盐酸 ⑨A12(SO4)3 ⑩KHSO4
(1)按物质的分类方法填写表格的空白处(填写序号):
| 分类标准 | 氧化物 | 非电解质 |
| 属于该类的物质 |
写出④在水中的电离方程式为______.
(2)写出下列物质相互之间反应的离子方程式:⑤+⑨______
②(过量)通入浑浊的⑥溶液后变澄清______
(3)经测定0.1mol/L⑩的水溶液与0.1mol/L⑧中的氢离子浓度基本相同,往固体①中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是______.
(4)③与⑦发生反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有19.2gCu发生反应时,转移电子的物质的量为______mol,产生的NO在标准状况下的体积为______L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com