
科目: 来源:2011届河南省普通高中毕业班高考适应性测试试卷(理综)化学部分 题型:填空题
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
请回答下列问题:
(1)B、C、D三种元素的电负性由大到小的顺序是 (填元素符号)。
(2)在A元素与上述其他元素形成的分子中,其中心原子为sp3杂化的分子式为 。(写出2种即)
(3)与C同族、且位于第四周期元素所形成气态化物的电子式为 ,它属于 (填“极性”或“非极性”)分子,其沸点低于C的氢化物的沸点,主要原因是 。
(4)F的基态原子核外电子排布式是 。
(5)E原子的第一电离能比同周期后面相邻元素的第一电离能 (填“大”或“小”)。
(6)氢气是理想的清洁能源,X元素与镧(La)元素的合金可做储氢材料,该合金的晶胞如右图所示,晶胞中心有一个X原子,其他X原子都在晶胞面上,则该晶体的化学式为 。已知该晶体的密度为 ,其摩尔质量为
,其摩尔质量为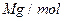 ,则该晶胞的体积是 。(请列出算式)
,则该晶胞的体积是 。(请列出算式)
查看答案和解析>>
科目: 来源:2011届浙江省绍兴一中高三下学期回头考试(理综)化学部分 题型:填空题
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
| | ⅠA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | | | ② | ④ | |
| 3 | ⑤ | | ③ | | | ⑥ | ⑦ | |

查看答案和解析>>
科目: 来源:2011届河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素,其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的+3价离子的3d能级为半充满状态。(答题时用ABCDE对应的元素符号表示)
(1)A的氢化物A2H2分子的空间构型为__________,其中心原子采取的杂化形式为___________,分子中含有___________个 键,__________π键。
键,__________π键。
(2)写出化合物DC的电子式_______,E原子的核外电子排布式________。
(3)由E元素形成的金属的晶胞结构如右图,则该晶胞中含有金属原子的数目为_______________。
(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于__________(填晶体类型)。
查看答案和解析>>
科目: 来源:2011届浙江省杭州市高三第二次质检(理综)化学部分 题型:填空题
(14分)
I.有A、B、C、D四种短周期元素,其中A、D同主族;又已知B和A可形成组成为BA的化合物,其中A的化合价为-1,B和C可形成组成为B2C2的化合物,A、B、C形成的单核离子的核外电子总数相同。
(1)元素A在周期表中的位置是 。
(2)B、C、D可形成组成为BDC的化合物,该化合物水溶液中通入过量CO2发生反应的离子方程式为 。
(3)B2C2在酸性条件下可形成具有二元弱酸性质的物质,该弱酸性物质和B的最高价氧化物对应水化物反应时可生成一种酸式盐,该酸式盐的电子式为 。
II.长期以来一直认为氟的含氧酸不存在。但是自1971年斯图杰尔和阿佩里曼(美)成功地合成了次氟酸后,这种论点被剧烈地动摇了。他们是在0℃以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。已知次氟酸的分子构成与次氯酸相仿。
⑴次氟酸中氧元素的化合价为 。
⑵下面给出了几个分子和基团化学键的键能(E):
| | H2 | O2 | F2 | O-H | O-F | H-F |
| E/(kJ/mol) | 432 | 494 | 155 | 424 | 220 | 566 |
查看答案和解析>>
科目: 来源:2010—2011学年福建省四地六校高二下学期第一次月考化学试卷 题型:填空题
(12分)图表法、图象法是常用的科学研究方法。请回答以下问题
(1)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。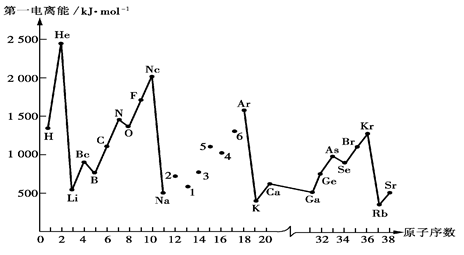
① 将Na—Ar之间六种元素用短线连接起来(不必写在答题卷上),构成完整的图像。从上图分析可知,同一主族元素原子的第一电离能I1变化规律是;__________________
_________________________________________________________________________
②上图折线中数字5代表元素在周期表中的位置是___________________________;
(2)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:试结合元素周期律知识完成下列问题:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | |
 当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是____________________(填离子键或共价键)。
当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是____________________(填离子键或共价键)。
查看答案和解析>>
科目: 来源:2010—2011学年福建省四地六校高二下学期第一次月考化学试卷 题型:填空题
(14分)请回答下列问题:
(1)下列现象和应用与电子跃迁无关的是________________________________。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱 E.石墨导电
(2)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。某平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有_______个σ键。
(3)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有______(填元素符号),
②在a:苯 b:CH3OH c:HCHO d:CS2 e:CCl4 五种有机溶剂中,碳原子采取sp3杂化的分子有___________(填字母),CS2 分子的键角是__________。
分子的键角是__________。
③过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如 [Co(H2O)6]2+显粉红色。其中Co2+的价电子排布式为________________________
[Co(H2O)6]2+显粉红色。其中Co2+的价电子排布式为________________________
(4)利用CO可以合成化工原料COCl2,其中
①COCl2分子的结构式为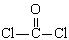 ,②COCl2分子内含有 (填标号);
,②COCl2分子内含有 (填标号);
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键 D.3个σ键、1个π键
查看答案和解析>>
科目: 来源:2010—2011学年福建省四地六校高二下学期第一次月考化学试卷 题型:填空题
(12分)按要求填空
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意 图是 ,第一电离能最小的元素的原子轨道表达式_______________________。
图是 ,第一电离能最小的元素的原子轨道表达式_______________________。
(2)第四周期元素中,4p轨道半充满的元素是_____________(填元素符号)
价电子层中s电子数与d电子数相同的元素是 (填元素名称)。
(3)中国古代四大发明之一――黑火药,它的爆炸反应方程式为:
2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除K、S外,上述方程式中出现的元素形成氢化物的稳定性从大到小依次为_____。
②写出K的基态电子排布式_____________________ _________________
_________________
查看答案和解析>>
科目: 来源:2011届吉林省高考复习质量监测(理综)化学部分 题型:填空题
(15分)
M、N、R、T为周期表中前四周期相邻两个周期的元素,且原子序数依次增大。已知T的次外层上电子没有排满,且该能层中成对电子数等于其它各能层上电子的总数;R和T在同一族;N的外围电子总数为6,均为未成对电子。根据以上信息,回答下列问题:
(1)T的元素符号为 ,在周期表中位于 族,N的价电子排布式为 。
(2)M和R两种元素组成的常见化合物有两种,其中一种可以单质之间进行化合,生成R的高价态化合物,请写出该反应的化学方程式: 。
(3)表面上附着氮原子的R可做为工业催化剂,下图为氮原子在R的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表R原子)。则图示颗粒表面上氮原子与R原子的个数比为 。
(4)T、N都有多种配合物,[T(NH3)3(H2O)M2]M是T配合物的一种,其中心离子的化合价为 ,配位数为 。N与甲基丙烯酸根的配合物为: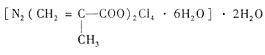 该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
查看答案和解析>>
科目: 来源:2010—2011学年四川省乐山一中高一下学期第一次月考化学试卷 题型:填空题
A、B、C三种主族元素在周期表中的位置相邻,它们的原子序数 依次增大。A、B原子的电子层相同,B、C原子的最外层电子数相同。已知三种元素
依次增大。A、B原子的电子层相同,B、C原子的最外层电子数相同。已知三种元素 原子的最外层电子数之和为17,质子数之和为31。
原子的最外层电子数之和为17,质子数之和为31。
写出:(1)A单质的电子式为 ;(2)B氢化物的结构式为 ;
(3)用电子式表示C氢化物的形成过程 。
查看答案和解析>>
科目: 来源:2010—2011学年四川省乐山一中高一下学期第一次月考化学试卷 题型:填空题
①日本核辐射含有一种碘(127I)的 131I(填“同种原子”或“同位素”或“同素异形体”)。人体缺碘容易引发甲状腺肿大,已知碘与氯同主族,周期序数比氯大2,则其原子序数为 ,其最高价氧化物的化学式为 ,对应水化物的化学式 。
②按已知的原子结构规律,116号元素应是第 周期第 族元素,它属于 元素(填“金属”或“非金属”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com