
科目: 来源:2010-2011学年山西省临汾一中高二下学期期中考试化学试卷 题型:填空题
(15分)下表是长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于 晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。
晶胞的体心、顶点、面心),则该化合物的化学式为 (用对应的元素符号表示)。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石 油化工发展水平的标志。有关该氢化物分子的说法正确的是
油化工发展水平的标志。有关该氢化物分子的说法正确的是  。
。
a.分子中含有氢键 b.属于非极性分子
c.含有4个σ键和1个π键 d.该氢化物分子中,②原子采用sp2杂化
(4)某元素的外围电子排布式为nsnnpn+1,该元素可与①形成三角锥形的分子X, X在①与③形成的分子Y中的溶解度很大,其主要原因是
。
(5)将过量的X通入含有元素⑩的硫酸盐溶液中,现象是 ,反应的离子方程式_ 。
(6) ⑩单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
若已知⑩的原子半径为d,NA代表阿伏加德罗常数,⑩的相对原子质量为M,请回答:晶胞中⑩原子的配位数为________,该晶体的密度为___ _____(用字母表示)。
查看答案和解析>>
科目: 来源:2010-2011学年山西省临汾一中高二下学期期中考试化学试卷 题型:填空题
(9分)请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有 种。
(2)请写出Cr元素的核外电子排布式 。
(3)某元素的正三价离子的3d能级为半充满,该元素的元素名称为 ,其单质在一定条件下能与S反应,试写出该反应的化学方程式 。
(4)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布图为 。
查看答案和解析>>
科目: 来源:2010-2011学年江苏省如皋市五校高二下学期期中调研化学试卷 题型:填空题
(12分)零排放、太阳能、绿色光源等高科技点亮2010上海世博。
⑴世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中的下列物质属于由极性键形成的非极性分子的是 。
a.CO b.NO c.NO2 d.CO2
⑵“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含Na、81Tl、49In、Sc、I等元素的单质或化合物。有关说法正确的是 。
a.第ⅢA元素铊和铟,第一电离能Tl小于In
b.元素Sc位于周期表s区
c.钠的熔点低,是因为金属键较弱
d.碘的电负性大于氯
⑶世博锗广泛采用了冰蓄冷空调。冰蓄冷空调采用液态化合物乙二醇(HOCH2CH2OH)介质,乙二醇沸点高, 是由于 。
是由于 。
⑷上海城区大规模集中使用“2l世纪绿色光源”LED半导体照明,LED晶片采厢砷化镓(GaAs)等材料组成。其中Ga 原子在基态时,其价电子轨道表示式为: 。GaAs的晶胞结构如图(As位于顶点和面心),晶胞中与As原子等距离且最近的Ga原子有 个。
原子在基态时,其价电子轨道表示式为: 。GaAs的晶胞结构如图(As位于顶点和面心),晶胞中与As原子等距离且最近的Ga原子有 个。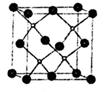
⑸“东方之冠”(中国馆)表面装有7000多块红色铝板,红色铝板为新型氟碳喷涂型材,一种氟碳涂层聚脂(FEP),它的单体为CF3-CF=CF2,该分子中碳原子的杂化方式有: 。
查看答案和解析>>
科目: 来源:2010-2011学年江苏省如皋市五校高二下学期期中调研化学试卷 题型:填空题
(12分)元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
⑴第四周期过渡元素的明显特征是形成多种多样的配合物。
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
⑵第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
⑶用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
a.直线形;三角锥形 b.V形;三角锥形
c.直线形;平面三角形 d.V形;平面三角形
⑷Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
①Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 (填晶体类型)。
②CuSO4·5H2O(胆矾)中含有水合铜离子因而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来) 。
查看答案和解析>>
科目: 来源:2010-2011学年江苏省如皋市五校高二下学期期中调研化学试卷 题型:填空题
(12分)下表是元素 周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | | |||||
| 二 | | | | ② | ③ | ④ | |
| 三 | ⑤ | | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 ,沸点高低
,沸点高低  +1价含氧酸的结构式
+1价含氧酸的结构式 查看答案和解析>>
科目: 来源:2011届山西省介休十中高三下学期模拟考试(理综)化学部分 题型:填空题
(15分)下表是元素周期表的一部分,用元素符号或化学式回答下列问题:
| 主族周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | | | | | | | | ① |
| 2 | | | | | ② | ③ | ④ | |
| 3 | ⑤ | ⑥ | ⑦ | | ⑧ | ⑨ | ⑩ | |
| 元 素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
查看答案和解析>>
科目: 来源:2011届陕西省西安市高三第三次质检(理综)化学部分 题型:填空题
A、B、C、D、E、F、G、H八种元素都是前4周期元素,且原子序数依次增大。
已知:元素A的原子中没有成对电子。
元素B、C、D同周期,元素B、G同主族,且B、D、G三原子P轨道上均有2个未成对电子
元素E、F、G在同一周期,且E原子中没有未成对电子。
元素H的基态原子核外有6个未成对电子。
请回答下列问题:
(1)B、C、D三元素的电负性由大到小排列顺序为 (用元素符号表示);E、F、G三元素的原子的第一电离能由大到小排列顺序为 (用元素符号表示)。
(2)元素D与G所形成的晶体和元素D与B所形成的晶体熔沸点由高到低的顺序为 (填化学式),其原因是 。
(3)元素B与C的气态氢化物在A B中溶解性由大到小的顺序为 (填化学式),其原因是 。
B中溶解性由大到小的顺序为 (填化学式),其原因是 。
(4)B、D两元素形成的阴离子BD 中的B的杂化类型为 ,空间结构为 ,与BD
中的B的杂化类型为 ,空间结构为 ,与BD 互为等电子体且含C、D两元素的微粒的化学式为 。
互为等电子体且含C、D两元素的微粒的化学式为 。
(5)A、B、C三元素各一个原子形成的分子中 键与
键与 键的个数比为 ,该分子的VSERR模型 。
键的个数比为 ,该分子的VSERR模型 。
(6)元素H的基态原子的核外电子排布为 ,在周期表中处于 区。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省宁海县正学中学高一下学期第二次阶段性测试化学试卷 题型:填空题
(12分)用“大于”或“小于”或“等于”回答下列问题:
(1)酸性:H2CO3 H2SiO3, H2SiO3 H3PO4
(2)碱性:Ca(OH)2 Mg(OH)2, Mg(OH)2 Al(OH)3
(3)气态氢化物稳定性:H2O H2S, H2S HCl
(4)还原性: H2O H2S, H2S HCl
(5)酸性: H2SO4 H2SO3, HClO4 HClO
从以上答案中可以归纳出:
①元素的非金属性越强,其对应最高价氧化物水化物的酸性越 ;
②元素的金属性越强,其对应最高价氧化物水化物的碱性越 。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省宁海县正学中学高一下学期第二次阶段性测试化学试卷 题型:填空题
(8分)由以下一些微粒: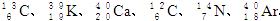 。其中:
。其中:
(1)互为同位素的是________和________;
(2)质量数相等,但不能互称同位素的是________和__________;
(3)中子数相等,但质子数不相等的是______和____ _、______和___ _。
查看答案和解析>>
科目: 来源:2010-2011学年河南省长葛市天阳中学高一下学期期中考试化学试卷 题型:填空题
在14 6C、14 7N、16 8O、3517CL、235 92U、238 92U中;
(1)____________和_____________互为同位素;
(2)___________和______________的质量数相等,但不能互称为同位素;
(3)___________和______________的中子数相等,但质子数不相等,所以不是同一种元素;
(4)以上所列共有_____________种元素;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com