
科目: 来源:2011-2012学年福建省晋江市季延中学高二上学期期末考试化学试卷 题型:填空题
(10分)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 基态原子核外电子共占据5个原子轨道且有2个未成对电子, |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| | A-B | A=B | A≡B |
| CO | 357.7 | 798.9 | 1071.9 |
| Y2 | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
科目: 来源:2011-2012学年宁夏中卫市海原一中高二第二学段考试化学试卷 题型:填空题
(17分)有A、B、C、D、E、Q六种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E均比A多一个电子层,且B、C、D、E是连继相邻的四种元素,其中E是元素周期表中非金属性最强的一种元素,Q的核电荷数是A、B、D、E的核电荷数的总和,按要求完成下列问题:
⑴.这几种元素中电负性最大的是( )(填元素符号,下同);
⑵.B、C、D、E的第一电离能由小到大的顺序是( ),原子半径由大到小的顺序是( );
⑶.C的氢化物的电子式是( ),C的氢化物结构式是( ),C的最高价氧化物对应的水化物的化学式是( ),C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是( );
⑷.Q的电子排布式是( ),Q的价电子排布式是( ),Q的价电子排布图是( )。
⑸.说出D、Q在周期表中的分区,D在( )区,Q在( )区, D原子核外有( )个成单电子.
⑹.元素B在周期表中位于第( )周期,第( )族。
查看答案和解析>>
科目: 来源:2011-2012年度上海市吴淞中学高二第一学期期末考试化学试卷 题型:填空题
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;下图是元素周期表的一部分,编号为③的元素最外层与最内层电子数等
(1)编号为⑤的元素的符号为 ,其在周期表中位于 。
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式: 。
(3)己知AlCl3的熔点为190 ℃(2.5×105Pa),沸点为182.7℃,
试推测:
①BeCl2是 化合物(填“离子”或“共价”),
②Be(OH)2的碱性比LiOH 。
(4)根据Mg在空气中的燃烧情况, Li在空气中燃烧生成的产物为 __(用化学式表示)。
查看答案和解析>>
科目: 来源:2012届甘肃省兰州一中高三上学期期末考试理综试卷(化学部分) 题型:填空题
(15分)下表是元素周期表的一部分,A、B、C、D、E、X、Y是表中给出元素组成的常见单质或化合物。
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
(1)若E为单质气体,D为白色沉淀, C与X反应的离子方程式为 。
(2)若E为氧化物,则A的化学式为 ,A与水反应的化学方程式为 。
①当X是显碱性的盐溶液,C分子中有22个电子时,则C的电子式为 ,表示X呈碱性的离子方程式为 。
②当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为 。
查看答案和解析>>
科目: 来源:2011-2012学年甘肃兰州一中高二上学期期末考试化学试卷 题型:填空题
(10分)1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
查看答案和解析>>
科目: 来源:2012届山东省潍坊市高三上学期期末考试化学试卷 题型:填空题
(13分)安全气囊是行车安全的重要设施。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、0四种元素。
(1)氧元素在元素周期表中的 位置是 ,Na原子结构示意图为 ,其中三种主族元素的离子半径从大到小的顺序是 (用离子符号表示)
位置是 ,Na原子结构示意图为 ,其中三种主族元素的离子半径从大到小的顺序是 (用离子符号表示)
(2)水溶性实验表明,安全气囊中固体粉末部分溶解。不溶物为一种红棕色固体,可溶于盐酸。已知该不溶物能发生铝热反应,写出反应的化学方程式 。
(3)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是 ,其水溶液显 性(填“酸”、“碱”或“中”),原因是
 (用离子方程式表示)。
(用离子方程式表示)。
查看答案和解析>>
科目: 来源:2012届内蒙古巴彦淖尔市中学巴市一中高三上学期12月月考理综试卷(化学部分) 题型:填空题
(16分)A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处于同一周期,A、C处于同一主族。C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的4倍。试回答下列问题:
(1)这四种元素分别是:A ,B ,C ,D 。
(2)这四种元素中能形成的气态氢化物的稳定性由大到小的顺序是
。(用气态氢化物的化学式表示)
(3)A和B形成的三原子分子的化学式是 ,B与D形成的既有离子键又含有共价键的化合物的化学式是 。
(4)A元素的某氧化物与D元素的某含氧化合物反应生成单质的化学方程式是
。
查看答案和解析>>
科目: 来源:2011-2012学年山东济宁鱼台二中高二上学期期末考前模拟化学试卷 题型:填空题
.(14分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| A | | | |||||||||||||||
| B | | | | C | D | E | F | | |||||||||
| G | H | I | J | | K | L | | ||||||||||
| | | | | | M | | | N | | | | | | | | | |
查看答案和解析>>
科目: 来源:2011-2012学年黑龙江哈尔滨市第六中学高三上学期期末考试化学试卷 题型:填空题
(10分)A、B、C三种短周期元素在周期表中相对位置如右图:
| A | | | |
| | | B | C |
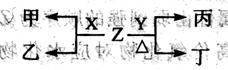
查看答案和解析>>
科目: 来源:2012届江西省南昌市高三调研测试化学试卷 题型:填空题
(10分)A、B、C、D、E原子序数依次递增的五种短周期元素,已知:
①B原子核外电子总数与最外层电子数之比为4:3
②D原子最外层电子数与次外层电子数之比为3:4
③E-,C+,A+的离子半径逐渐减小
④A单质在E单质中燃烧火焰呈苍白色
请回答下列问题:
(1)E的最高价氧化物对应水化物的化学式为:___________。它的酸性比D的最高价氧化物对应水化物的酸性:____________。(填“强”或“弱”)
(2)X、Y是由上述元素中任意3种组成的强电解质,且构成的原子个数比均为1:1:1。已知X溶液中水电离出来的C(H+)=10-12mol/L,则X的电子式为:_____________;Y的水溶液酸碱性与X相同,则其原因是(写离子方程式):_______________________________;
(3)B与C构成原子个数比为1:1的化合物与H2O反应的化学方程式为:__________________________________________;
(4)A与B,A与D均可形成18个电子的分子,这两种分子在水溶液中反应生成物之一是含10电子的化合物;该反应可观察到现象是:____________________________________,原因是(用化学方程式表示)_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com