
科目: 来源:2012-2013学年河南郑州盛同学校高一下学期第一次月考化学试卷(带解析) 题型:填空题
已知A、B、C、D、E属于原子序数依次增大的短周期主族元素。短周期元素中C元素的原子半径最大,A的原子半径最小。B元素能形成一种碱性气体。E元素原子的最外层电子数是次外层电子数的一半,且在周期表中与D元素相邻。
(1)写出3种元素的名称:C________ 、D_________、 E___________。
(2)写出D元素在周期表中的位置:__________________________。
(3)画出C元素原子的结构示意图:____________________。
(4)写出D、E的氧化物分别与强碱溶液反应的离子方程式:
___________________________________________;
___________________________________________。
(5)A、B两元素能形成一种5核10电子的阳离子,请叙述实验室检验溶液中的该离子的操作方法:___________________________________________
____________________________________________________。
查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
Q、R、X、Y、Z 为前 18 号元素中的五种,Q 的低价氧化物与 X 单质分子的电子总数相等,R 与 Q 同族,X、Y与Z不同族,Y 和 Z 的阴离子与 Ar 原子的电子结构相同且 Y 的原子序数小于 Z。
(1)Q 的最高价氧化物,其固态俗名叫____________;
(2)R 的氢化物分子的空间构型是_____________,它与 X 形成的化合物可作为一种重要的陶瓷材料,其化学式是_____________;
(3)X 的常见氢化物的空间构型是_____________;它的另一氢化物 X2H4是一种火箭燃料的成分,其电子式是___________________;
(4)Q 分别与 Y、Z 形成的化合物的化学式是_____________和____________;Q和 Z 形成的化合物分子的结构式是_____________________,属于____________化合物(填“离子”或“共价”)。
查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
| X | Y | Z | |
| | R | | |
| | | W | |
| | | | J |
查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
(1)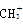 、—CH3、
、—CH3、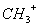 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________
| A.它们均由甲烷去掉一个氢原子所得 |
| B.它们互为等电子体,碳原子均采取sp2杂化 |
| C.CH与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
D.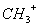 中的碳原子采取sp2杂化,所有原子均共面 中的碳原子采取sp2杂化,所有原子均共面 |
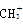 和一个
和一个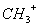 结合均可得到CH3CH3
结合均可得到CH3CH3查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2等)与 H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有 Cu、Zn、Al 等元素。写出基态 Cu2+离子的核外电子排布式_______________________________________;
(2)根据等电子原理,写出 CO 分子的结构式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛与新制 Cu(OH)2的碱性溶液反应生成 Cu2O 沉淀。
①甲醛分子中碳原子轨道的杂化类型为_____________________;
②甲醛分子的空间构型是__________________;
③ 1 mol 甲醛分子中 σ 键的数目为__________________。
查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
(1)中国古代四大发明之一——黑火药,它的爆炸反应为:
2KNO3+ 3C+S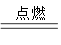 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
① 除 S 外,上列元素的电负性从大到小依次为_________________________;
②生成物中,A 的电子式为__________________ ,含极性共价键的分子的中心原子轨道杂化类型____________;
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布式为_______________________________,Q2+的未成对电子数是________。
查看答案和解析>>
科目: 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
(1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有______种,原子中所有电子占有______个轨道,核外共有_________个不同运动状态的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_____________。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是______,F2-的电子排布式是_______________________________。
(4)M能层上有____个能级,有____个轨道,作为内层最多可容纳______个电子,作为最外层时,最多可含有______个未成对电子。
(5)在元素周期表中,最外层只有1个未成对电子的主族元素原子处于________________族;最外层有2个未成对电子的主族元素原子处于__________________族。
查看答案和解析>>
科目: 来源:2012-2013学年新疆乌鲁木齐一中高一(特长班)下期中考试化学卷(带解析) 题型:填空题
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)①在元素周期表中的位置是(周期、族) ;
(2)比较④和⑦的氢化物的稳定性(用化学式表示) 。
查看答案和解析>>
科目: 来源:2012-2013学年新疆乌鲁木齐一中高一(特长班)下期中考试化学卷(带解析) 题型:填空题
下表是元素周期表的一部分。根据表中的10种元素,用元素符号或化学式填空:
| 族 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | | | | | | | |
| 2 | | | | ② | | ③ | | |
| 3 | | | ④ | ⑤ | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | ⑩ | |
查看答案和解析>>
科目: 来源:2013届浙江省嘉兴市高三上学期基础测试化学试卷(带解析) 题型:填空题
X、Y、Z、D、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX,ZX焰色反应为黄色;Y、D同主族,可形成DY2、DY3两种分子。请回答下列问题:
(1)D在元素周期表中的位置为为 。Y、Z、D的原子半径由大到小的顺序 (用元素符号表示)。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是 (写化学式)非金属气态氢化物中述原性最强的是 (写化学式)。
(3)由Y、G两元素形成的可作饮用水消毒剂的化合物的是 (写化学式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com