
科目: 来源:09~10年南京六中高二下学期期末考试 题型:填空题
(22分) 乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1) CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ;1mol O22+中含有的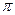 键数目为 。
键数目为 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2,红棕色沉淀。Cu+基态核外电子排布式为 。
(3)乙炔与氢氰酸反应可得丙烯腈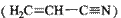 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
(4) CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为 。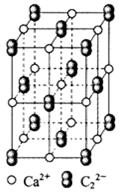
(5)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛高,其主要原因是 ;甲醛分子中碳原子的轨道杂化类型为 。
②甲醛分子的空间构型是 ;1mol甲醛分子中σ键的数目为 。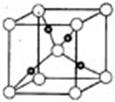
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为 。
查看答案和解析>>
科目: 来源:09~10年宝鸡中学高二下学期期末考试化学卷 题型:填空题
(10分)某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: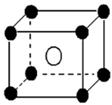
(1)晶体中Y的配位数是 ; X的配位数是 ;该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有 个。
(3)该晶体的摩尔质量为M g/mol,晶体密度为ρ g/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。
查看答案和解析>>
科目: 来源:09~10年建湖二中高二下学期期末考试化学卷 题型:填空题
(共计12分)
A.锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基
态电子排布式 ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为 ;
在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键 。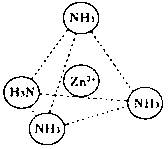
(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;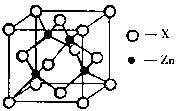
该化合物的晶体熔点比干冰高得多,原因是 。
查看答案和解析>>
科目: 来源:2010年安丘中学高二暑期练习化学卷(三) 题型:填空题
如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。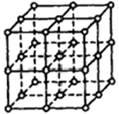
(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有 个。
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为 cm。计算过程如下:
。
查看答案和解析>>
科目: 来源:2010年厦门一中高二暑期水平测试 题型:填空题
金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为R ,摩尔质量为M,阿伏加德罗常数为NA,求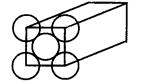
(1)金晶体中最小的一个立方体含有__________个金属原子。
(2)金的密度为_________g·cm-3。
查看答案和解析>>
科目: 来源:2010届河北沙河一中考前热身理综化学卷(二) 题型:填空题
[选修物质结构].铁是地球表面最丰富的金属之一,能形成多种配合物,铁系催化剂是工业生产中常用的催化剂。
(1)合成氨工业使用的催化剂是以铁为主体的多成分催化剂。
①NH3中N原子的杂化轨道类型是 。
②N与O同属第二周期,N的第一电离能比O大的原因是 。
③根据等电子体原理,写出一种NH4+是等电子体的微粒的化学式____________。
(2)二茂铁[(C5H5)2Fe]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右所示,其中氢原子的化学环境完全相同。
①Fe的基态电子排布式为____________。
②二茂铁中Fe2+与环戊二烯离子(C5H5-)之间的化学键类型是 _______________。
③1mol环戊二烯( )中含有σ键的数目为_________个。
)中含有σ键的数目为_________个。
(3)普鲁士蓝俗称铁蓝,结构如图所示,K+未画出),每隔一个立方体在立方体中心含有一个K+离子,普鲁士蓝中铁元素的化合价有+2和+3两种,其中Fe3+与Fe2+的个数比为:_____________。
查看答案和解析>>
科目: 来源:2009—2010泉州七中学年度下学期高二年期中考试化学卷 题型:填空题
(8分) 现有下列晶体, 请按要求回答相应问题。(前六个小题用编号填空)
| A.干冰 | B.晶体硅 | C.氩 | D.二氧化硅 E.氯化铵 |
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题六 物质结构和元素周期律 题型:填空题
(1)中国古代四大发明之一——黑火药,它的爆炸反应为:

①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 ,含极性共价键的分子的中心原子轨道杂化类型为 。
③已知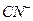 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为 。
键数目之比为 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,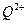 的未成对电子数是 。
的未成对电子数是 。
(3)在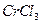 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为 (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
交换出来的 经中和滴定,即可求出x和n,确定配离子的组成。
经中和滴定,即可求出x和n,确定配离子的组成。
将含0.0015 mol  的溶液,与R-H完全交换后,中和生成的
的溶液,与R-H完全交换后,中和生成的 需浓度为0.1200 mol
需浓度为0.1200 mol NaOH溶液25.00 ml,呆知该配离子的化学式为 。
NaOH溶液25.00 ml,呆知该配离子的化学式为 。
查看答案和解析>>
科目: 来源:2010届湖北省黄冈中学高三11月月考化学测试卷 题型:填空题
(5分)德国和美国科学家首次制造出了由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成的(如图所示)。请回答:
C20分子中共有 个正五边形,共有 条棱边。
C20晶体属于 (填晶体类型)。
查看答案和解析>>
科目: 来源:2010年厦门双十中学高三考前热身卷理科综合(化学) 题型:填空题
[化学——物质结构与性质](13分)
(1)金属钛(22Ti) 将是继铜、铁、铝之后人类广泛使用的第四种金属,写出Ti元素的基态原子电子排布式为 ;
(2)日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电子数为 。
(3)COCl2俗称光气,分子中C原子采取 杂化成键;其中碳氧原子之间的共价键含有 (填字母): a.2个σ键;b.2个π键;c.1个σ键、1个π键。
(4)①短周期某主族元素M的逐级电离能情况如下图A所示,则M元素位于周期表的第
族。
②第三周期8种元素按单质熔点高低的顺序如下图B所示,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填图B中的序号)。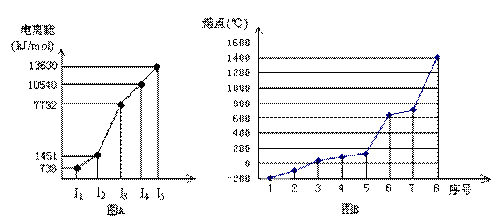
(5)由C原子跟Si原子以1 : 1相互交替结合而形成的晶体,晶型与晶体Si相同。两者相比熔点更高的是 (填化学式)试从结构角度加以解释: 。
(6)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com