
科目: 来源:2010年沙河一中考前预测卷化学试题 题型:单选题
关于下列四个图像的说法中正确的是

A.图①表示可逆反应“A2(g)+B2(g) 2AB3(g)”的ΔH大于0 2AB3(g)”的ΔH大于0 | B.图②是在电解氯化铜稀溶液的电解池中,阴、阳极产生气体的物质的量之比一定为1:1  | C.图③表示可逆反应“CO(g) + H2O(g) CO2(g)+H2(g)”中的ΔH大于0 CO2(g)+H2(g)”中的ΔH大于0  | D.图④表示压强对可逆反应2A(g)+B(g) 3C(g)+D(s)的影响,甲的压强大 3C(g)+D(s)的影响,甲的压强大 |
查看答案和解析>>
科目: 来源:2010届陕西留坝中学高三模拟考试化学卷 题型:单选题
下列说法不正确的是( )
| A.化学反应是旧键断裂和新键形成的过程 |
| B.盖斯定律实质上是能量守恒定律的体现 |
| C.反应前后分子数发生改变的反应不遵循质量守恒定律 |
| D.溶解平衡、水解平衡和电离平衡均为动态平衡 |
查看答案和解析>>
科目: 来源:2010年湖南省普通高中学业水平考试化学卷 题型:单选题
下列有关反应的能量变化,错误的是
| A.化学反应中,有放热反应也有吸热反应 |
| B.化学反应中的能量变化主要由化学键的变化引起的 |
| C.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应是放热反应 |
| D.盐酸与NaOH溶液的反应是放热反应 |
查看答案和解析>>
科目: 来源:2010年长沙市一中学业水平模拟测试卷(三)化学卷 题型:单选题
下列关于化学反应与能量的说法正确的是
| A.燃烧反应不一定是放热反应 |
| B.化学反应一定既有物质变化又有能量变化 |
| C.反应物断键所吸收的总能量高于生成物形成键所放出的总能量的反应为放热反应 |
| D.反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
查看答案和解析>>
科目: 来源:2010年长沙市一中学业水平模拟测试卷(三)化学卷 题型:单选题
下列反应中,是吸热反应的是( )
A.铝片与稀硫酸反应 B 乙醇在空气中燃烧
C.盐酸与氢氧化钠溶液反应 D 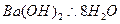 晶体与氯化铵晶体反应
晶体与氯化铵晶体反应
查看答案和解析>>
科目: 来源:2009—2010学年河北冀州中学高一下学期期中考试化学卷 题型:单选题
下列说法正确的是( )
| A.化学反应中的能量变化都表现为热量的变化 |
| B.吸热反应在不加热的条件一定不能发生 |
| C.需要加热才能发生的反应一定是吸热反应,放热反应在常温下一定很容易发生 |
| D.反应是吸热还是放热必须看旧键断裂时吸收的能量和新键生成时释放能量的大小 |
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题十四 化学计算 题型:单选题
已知 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
则表中a为
| A.404 | B.260 | C.230 | D.200 |
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题七 化学反应中的能量变化 题型:单选题
下列与化学反应能量变化相关的叙述正确的是
| A.生成物能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题八 化学反应速率和化学平衡 题型:单选题
下列有关化学研究的正确说法是
| A.同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| B.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
| C.依据丁达尔现象可将分散素分为溶液、胶体与浊液 |
| D.从HF、HCl、HBr、Hl酸性递增的事实,推出F、Cl、Br、l的非金属性递增的规律 |
查看答案和解析>>
科目: 来源:2009-2010学年乐亭一中高一第二学期期中化学试题 题型:单选题
1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是:
| A.C(s)+O2(g)=CO2(g);△H =" +393.5" kJ?mol-1 |
B.C(s)+ O2(g)=CO(g);△H = -393.5 kJ?mol-1 O2(g)=CO(g);△H = -393.5 kJ?mol-1 |
| C.C+O2=CO2;△H = -393.5 kJ?mol-1 |
| D.C(s)+O2(g)=CO2(g);△H = -393.5 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com