
科目: 来源:2011-2012学年江西省安福中学高二上学期期中考试化学试卷 题型:填空题
(10分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。根据右图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式___________。
(2)PCl5分解成PCl3和Cl2的热化学方程式__________,
(3)P和Cl2分两步反应生成1molPCl5的△H3=______,P和Cl2一步反应生成1molPCl5的△H4_______△H3 (填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是_____________________。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省江阴市一中高二上学期期中考试化学(选修)试卷 题型:填空题
(10分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256KJ的热量。
(1)反应的热化学方程式为 ___________________ 。
(2)又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 ______ KJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很 大的优点是 ________________________
大的优点是 ________________________  。
。
(4)已知N2(g) + 2O2(g) ="===" 2NO2(g) ΔH=+67.7kJ/mol
N2H4(g) + O2(g) ="===" N2(g) + 2H2O(g) ΔH=-534kJ/mol
则肼与NO2完全反应生成氮气和液态水的热化学方程式
。
查看答案和解析>>
科目: 来源:2011-2012年广东省广雅中学高二上学期期中考试化学(理)试卷 题型:填空题
(8分)甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备气态甲醛。甲醛与气态甲醇转化的能量关系如图所示: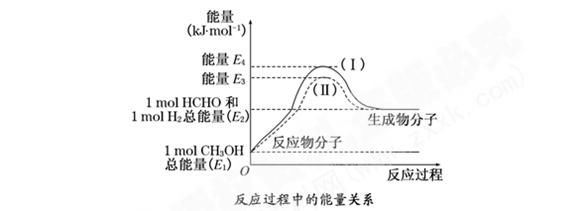
(1)甲醇催化脱氢转化为甲醛的反应是 (填“吸热”或“放热”)反应.
(2)过程Ⅰ与过程Ⅱ的反应热是否相同? ,理由是  。
。
(3)合成甲醇的主要反应为:CO(g)+2H2(g) CH3OH(g)△H<0,其化学平衡常数K和温度T的关系如下表所示:
CH3OH(g)△H<0,其化学平衡常数K和温度T的关系如下表所示:
| T/℃ | T1 | T2 | T3 |
| K | 1/1000 | 1/40 | 25 |
查看答案和解析>>
科目: 来源:2011-2012学年湖北省部分重点中学高二上学期期中联考化学试卷 题型:填空题
(11分)氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13. 8 8 |
 2NH3,2 min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=______________(用分数表示);欲使K增大,可以采取的措施是___________________。
2NH3,2 min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=______________(用分数表示);欲使K增大,可以采取的措施是___________________。
 2NH3(l) △H=___________。
2NH3(l) △H=___________。查看答案和解析>>
科目: 来源:2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷 题型:填空题
(12分)红磷P(s)和Cl2(g)发生反应生成 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________ ____
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目: 来源:2012届河北省唐山一中高三上学期期中考试化学试卷 题型:填空题
(10分)键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。参考以下表格的键能数据,回答下列问题:
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能 /kJ·mol-1 /kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
 ____________
____________查看答案和解析>>
科目: 来源:2012届安徽省望江县高三上学期第二次月考化学试卷 题型:填空题
(13分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH—、C1—、CO32—、NO3—、SO42— |
 能产生沉淀;C只能与D反应产生沉淀。
能产生沉淀;C只能与D反应产生沉淀。 。
。 的热化学方程式 。
的热化学方程式 。查看答案和解析>>
科目: 来源:2012届江西省九江一中高三第一次月考化学试卷 题型:填空题
(4分)(1)工业上Al2Te3可用来制备H2Te,完成下列化学方程式并配平:
( )Al2Te3+( ) 
( )Al( OH)3↓+( )H2Te↑
OH)3↓+( )H2Te↑
(2)在101kPa时,4.0g硫粉在氧气中完全燃烧生成SO2,放出37kJ的热量,则硫燃烧的热化学方程式为 。
查看答案和解析>>
科目: 来源:2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷 题型:填空题
(12分)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是_____________kJ;[来源:学+科+网]
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
下列说法正确的是______(填序 号)
号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为 v(CH3OH)=  mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为 ;
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为 、正极的反应式为 。
查看答案和解析>>
科目: 来源:2011-2012学年河北省唐山一中高二上学期期中考试化学(文)试卷 题型:填空题
(3分)已知某条件下,1molN2(气态)与适量H2 (气态)完全反应后生成 NH3(气态),放出92.2 kJ的热量,请写出该反应的热化学方程式:
______________ __________________________________________________
__________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com