
科目: 来源:2011-2012学年湖北省武汉市五校高二上学期期中统考化学试卷(带解析) 题型:单选题
在N2 +3H2 2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6 mol·L-1。此时间内用H2表示的平均速率为0.45 mol·L-1·s-1,则此段时间值是
2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6 mol·L-1。此时间内用H2表示的平均速率为0.45 mol·L-1·s-1,则此段时间值是
| A.1 s | B.2 s | C.0.44 s | D.1.33 s |
查看答案和解析>>
科目: 来源:2011-2012学年浙江湖州菱湖中学高二下学期期中考试化学试卷(带解析) 题型:单选题
可逆反应mA(g) nB(g)+pC(s);△H="Q," 温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图像,以下叙述正确的是
nB(g)+pC(s);△H="Q," 温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图像,以下叙述正确的是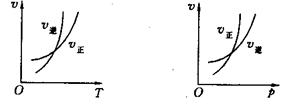
| A.m>n,Q>0 | B.m>n+p,Q>0 | C.m>n,Q<0 | D.m<n+p,Q<0 |
查看答案和解析>>
科目: 来源:2011-2012学年广东始兴县风度中学高二下学期期中考试理综化学试卷(带解析) 题型:单选题
在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则该反应的平均反应速率为()
| A.0.4mol/(L·s) | B.0.3mol/(L·s) | C.0.2mol/(L·s) | D.0.1mol/(L·s) |
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高二第二学期期中考试化学试卷(带解析) 题型:单选题
反应4NH3(g)+ 5O2(g)= 4NO(g)+ 6H2O(g)在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)可表示为( )
| A.v(NH3)=0.010mol???L-1?s-1 | B.v(O2)=0.0010mol???L-1?s-1 |
| C.v(NO)=0.0010mol???L-1?s-1 | D.v(H2O)=0.045mol???L-1?s-1 |
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高一第二学期期中考试化学试卷(带解析) 题型:单选题
在2A + B =" 3C" + 4D 的反应中,表示该反应速率最快的是( )
| A.vA=0.5 mol·(L·s)-1 |
| B.vB=0.3 mol·(L·s)-1 |
| C.vC=0.6 mol·(L·s)-1 |
| D.vD=1 mol·(L·s)-1 |
查看答案和解析>>
科目: 来源:2011-2012年浙江宁波万里国际中学高一第二学期期中考试化学试卷(带解析) 题型:单选题
在10L的容器中进行如下反应:N2 + 3H2 = 2NH3,3s后,NH3的物质的量增加0.12mol,用H2浓度的变化表示3s内的平均反应速率为( )
| A.0.003mol?(L?s)-1 | B.0.045 mol?(L?s)-1 |
| C.0.006 mol?(L?s)-1 | D.0.009 mol?(L?s)-1 |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市安宜高中高一下学期期中考试化学试卷(带解析) 题型:单选题
反应2A(g)+3B(g )=2C(g )+D(g )在四种不同情况下的反应速率如下,其中反应速率v最大的是:
A.v(A) =0.75mol/(L·s) B.v(B)=0.6mol/(L·s)
C.v(C)=1.0mol/(L·s) D.v (D) =0.8mol/(L·s)
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市安宜高中高一下学期期中考试化学试卷(带解析) 题型:单选题
已知某化学实验的结果如下表:
| 实验序号 | 反应物 | 在相同温度下测得的反 应速率v/mol·(L·min)-1 | |
| 大小相同的金属片 | 酸溶液 | ||
| 1 | 镁条 | 1 mol·L-1盐酸 | v1 |
| 2 | 铁片 | 1 mol·L-1盐酸 | v2 |
| 3 | 铁片 | 0.1 mol·L-1盐酸 | v3 |
查看答案和解析>>
科目: 来源:2012年普通高等学校招生全国统一考试理综化学部分(福建卷带解析) 题型:单选题
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是 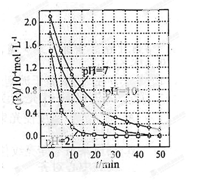
| A.在0-50min之间, pH ="2" 和 PH=" 7" 时 R 的降解百分率相等 |
| B.溶液酸性越强, R 的降解速率越小 |
| C.R的起始浓度越小,降解速率越大 |
| D.在 20-25min之间, pH =" 10" 时 R 的平均降解速率为 0.04mol·L-1·min-1 |
查看答案和解析>>
科目: 来源:2011-2012学年辽宁省东北育才学校高一下学期期中考试化学试卷(带解析) 题型:单选题
在373K时,把0.5摩N2O4气体通入为5升的真空密闭容器中,立即出现棕色,反应进行到2秒时,NO2的浓度为0.02摩/升,在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍,下列说法正确的是
| A.前2秒,以N2O4的浓度变化表示的平均反应速度为0.01摩/升·秒 |
| B.在2秒时体系内压强为开始时压强的1.1倍 |
| C.在平衡体系内含N2O40.25摩 |
| D.平衡时, N2O4的转化率为40% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com