
科目: 来源:2011年河南省卫辉市第一中学高二1月月考化学试卷 题型:单选题
当下列反应达到平衡时,保持温度不变,向容器中充入氩气,平衡一定不移动的是( )
A.N2(g)+3H2(g)  2NH3(g) 2NH3(g) | B.2HI(g)  H2(g)+I2(g) H2(g)+I2(g) |
C.PCl5(g)  PCl3(g)+Cl2(g) PCl3(g)+Cl2(g) | D.2SO2(g)+O2(g)  2SO3(g) 2SO3(g) |
查看答案和解析>>
科目: 来源:2011年河南省卫辉市第一中学高二1月月考化学试卷 题型:单选题
可逆反应N2(g)+3H2(g) 2NH3(g)的正逆反应速率可用各反应物或生物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
2NH3(g)的正逆反应速率可用各反应物或生物浓度的变化来表示。下列关系中能说明反应已达到平衡状态的是
| A.3v正(N2)= v正(H2) | B.v正(N2)= v正(NH3) |
| C.2v正(H2)="3" v逆(NH3) | D.v正(N2)="3" v逆(H2) |
查看答案和解析>>
科目: 来源:2011届重庆市重庆八中高三年级第四次月考理综化学部分 题型:单选题
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO 2CO2+N2。若利用飞机释放的NO和CO作为反应原料,在温度一定体积为10L的容器中反应,下列说法正确的是
2CO2+N2。若利用飞机释放的NO和CO作为反应原料,在温度一定体积为10L的容器中反应,下列说法正确的是
| A.若达平衡后充入稀有气体,体系压强增大,平衡将正向移动 |
| B.若升高温度可减少平衡体系中NO的浓度,则该反应△H > 0 |
| C.当体系中CO2和CO的浓度相等时,该反应达到平衡状态 |
| D.可以探索开发更加合适的催化剂,以提高尾气的转化率 |
查看答案和解析>>
科目: 来源:2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷 题型:单选题
一定温度和压强下,下列各可逆反应达到化学平衡状态,各反应有如图所示的对应关系: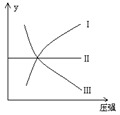
(1)N2(g)+3H2(g) 2NH3(g);ΔH<0(曲线Ⅰ)
2NH3(g);ΔH<0(曲线Ⅰ)
(2)H2(g)+I2(g) 2HI(g);ΔH>0(曲线Ⅱ)
2HI(g);ΔH>0(曲线Ⅱ)
(3)2SO3(g)  2SO2(g) +O2(g);ΔH>0(曲线Ⅲ)
2SO2(g) +O2(g);ΔH>0(曲线Ⅲ)
则下列y轴的表达意义均符合上述三个平衡状态的是
| A.平衡混合气中一种生成物的物质的量浓度 |
| B.平衡混合气中一种反应物的体积分数 |
| C.平衡混合气的平均相对分子质量 |
| D.平衡混合气中一种反应物的转化率 |
查看答案和解析>>
科目: 来源:2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷 题型:单选题
在一密闭容器中,反应mA(g )  nB(g) 达到平衡后,保持温度不变,改变容器体积(V)时,B的浓度变化如图所示,以下判断正确的是
nB(g) 达到平衡后,保持温度不变,改变容器体积(V)时,B的浓度变化如图所示,以下判断正确的是 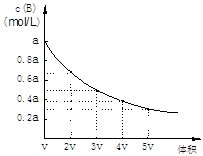
| A.物质B的质量分数增加 |
| B.平衡向逆反应方向移动 |
| C.物质A的转化率减小 |
| D.化学计量数:m>n |
查看答案和解析>>
科目: 来源:2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷 题型:单选题
在密闭容器中有可逆反应: 处于平衡状态(已知n+m>p),则下列说法正确的是
处于平衡状态(已知n+m>p),则下列说法正确的是
①升温,c(B)/c(C)的比值变小
②降温时体系内混合气体的平均相对分子质量变小
③加入B,A的转化率增大
④加入催化剂,气体总的物质的量不变
⑤加压使容器体积减小,A或B的浓度一定降低
⑥若A的反应速率为υA,则B的反应速率为υAn/m
A.①②③⑤ B.①②③④
C.①②⑤⑥ D.③④⑤⑥
查看答案和解析>>
科目: 来源:2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷 题型:单选题
下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡:Cl2+H2O HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅 HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅 |
B.对2HI(g)  H2(g)+I2(g),平衡体系增大压强可使颜色变深 H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
C.反应CO+NO2  CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
D.合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(N2+3H2 2NH3;DH<0) 2NH3;DH<0) |
查看答案和解析>>
科目: 来源:2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷 题型:单选题
可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是:
2NH3已达到平衡状态的是:
①一个N≡N键断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均式量不再改变
④保持其它条件不变时,体积压强不再改变
⑤NH3%、N2%、H2%都不再改变
⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2)=0.6mol/L·min,逆反应速率v(NH3)=0.4mol/L·min
⑧υ正(N2)=υ逆(NH3)
⑨2υ正(H2)=3υ逆(NH3)
| A.全部 | B.只有①③④⑤⑨ |
| C.②③④⑤⑦⑨ | D.只有①③⑤⑥⑦ |
查看答案和解析>>
科目: 来源:2011届湖北省补习学校高三联合体大联考理科综合化学部分 题型:单选题
将等物质的量的F2和ClF混合,在密闭容器中发生反应: F2(g)+ClF(g)  ClF3(g);△H<0。下列叙述中,正确的是
ClF3(g);△H<0。下列叙述中,正确的是
| A.恒温恒容时,当ClF 转化40% 时,容器内的压强为初始时的0.6 倍 |
| B.若 c(F2):c (ClF): c (ClF3) ="1:" 1: 1,则反应一定达到平衡状态 |
| C.达到平衡后,若增大容器容积,则正反应速率减小,逆反应速率增大,平衡左移 |
| D.平衡后再降低温度,保持恒容,达到新的平衡,则混合气体的平均摩尔质量增大 |
查看答案和解析>>
科目: 来源:2011届福建省福州金桥高级中学高三12月月考化学试卷 题型:单选题
在一定温度下,容器内某一反应中M、N的物质的量n随反应时间t变化的曲线如图所示,下列表述中正确的是
A.反应的化学方程式为2M N N |
| B.t2时V正=V逆,达到平衡 |
| C.t3时V正> V逆 |
| D.t1时浓度c(N)=2c(M) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com