
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
化学“多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生(整个反应只需要第一个反应发生,就好像多米诺骨牌游戏一样).以下就是一个化学“多米诺实验”,已知H2O2在MnO2的催化作用下可分解产生O2和H2O.如图所示A~H各装置中分别盛放的物质为:
A.稀硫酸;B.锌粒;C.3%H2O2溶液;D.MnO2 E.某溶液;F.CaCO3块状固体;G.滴有紫色石蕊的蒸馏水;H.足量澄清石灰水.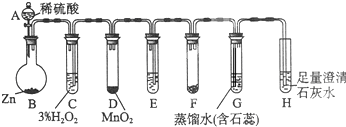
请回答以下各题:
(1)实验开始前必须进行的操作是______.
(2)反应开始后,若G中出现红色,H中有白色沉淀生成,判断E中的物质可能是______.(填名称)
(3)写出指定装置中发生反应的离子方程式.B.______;F.______;H.______.
(4)各装置中发生了氧化还原反应的是______(填装置编号).
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 单质 | 氧化物 | 酸 | 碱 | 盐 | |
| A | HD | 水 | 硫酸 | 烧碱 | 胆矾 |
| B | 黄铜 | NO2 | 盐酸 | 石灰水 | FeSO4 |
| C | 碘酒 | 一氧化碳 | 磷酸 | NH3?H2O | 食盐 |
| D | H2 | Fe3O4 | HNO3 | 纯碱 | 小苏打 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
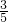 倍
倍查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作步骤 | 实验现象 |
| ______ | ______ |
查看答案和解析>>
科目: 来源: 题型:解答题
某溶液中可能含有SO32-、SO42-、HCO3-三种离子中的两种或三种.为探究其组成,小明取出两份相同的样品溶液于试管中,向一份中加入过量的盐酸,产生无色气泡;向另一份中滴加过量的氯化钡溶液,产生白色沉淀.请设计合理实验,做进一步的探究,对小明的实验给出结论.
仅限选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、集气瓶、铁架台、漏斗、滤纸、酒精灯、带单孔胶塞的导管;1mol/L硫酸;2mol/L盐酸;2mol/L硝酸、;1mol/L氯化钡、澄清石灰水、品红溶液、蒸馏水.
完成下列探究过程:
(1)提出假设:
假设1:溶液中存在SO32-、SO42-假设2:______;
假设3:______;假设4:溶液中存在SO32-、SO42-、HCO3-
(2)基于假设4,设计出实验方案,将实验操作、预期的实验现象和结论填在下表中.
[提示]I、在答题卡上按照下表的方式作答,注意前后内容的对应.
Ⅱ、注意文字简洁,超出答题卡空间视为无效.
III、可不填满,也可增加步骤.
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
| ③ | ||
| ④ | ||
| … | … | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com