
科目: 来源:2012届辽宁省辽南协作体高三上学期期中考试化学试卷 题型:单选题
将O2、NO、NH3、HCl分别收集于等体积的四个容器里,把四个容器用导管连成一个整体,若使各气体充分混合(保持温度 不
不 变),混合后容器中的压强与原容器中的压强之比为( )
变),混合后容器中的压强与原容器中的压强之比为( )
| A.1:1 | B.1:2 | C.3:4 | D.3:8 |
查看答案和解析>>
科目: 来源:2012届辽宁省辽南协作体高三上学期期中考试化学试卷 题型:单选题
在恒温、恒容下,发生如下反应:2A(g)+2B(g) C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2 mol·L-1;途径Ⅱ:C、D的起始浓度分别为2 mol·L-1和6 mol·L-1。以下叙述正确的是( )
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2 mol·L-1;途径Ⅱ:C、D的起始浓度分别为2 mol·L-1和6 mol·L-1。以下叙述正确的是( )
A.达到平衡时,途径Ⅰ的反应速率等于途径Ⅱ的反应速率
B.达到平衡时,途径Ⅰ所得混合气体的压强等于途径Ⅱ所得混合气体的压强
C.两途径最终达到平衡时,体系内各组分的百分含量相同
D.两途径最终达到平衡时,体系内各组分的百分含量不相同
查看答案和解析>>
科目: 来源:2012届辽宁省辽南协作体高三上学期期中考试化学试卷 题型:单选题
在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O(g)发生反应:CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
| A.在该温度下平衡常数K=1 | B.平衡常数与反应温度无关 |
| C.CO的转化率为50% | D.其他条件不变改变压强平衡不移动 |
查看答案和解析>>
科目: 来源:2012届辽宁省辽南协作体高三上学期期中考试化学试卷 题型:单选题
可逆反应N2(g)+3H2(g) 2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
| A.3v正(N2)=v正(H2) | B.v正(N2)=v逆(NH3) |
| C.2v正(H2)=3v逆(NH3) | D.v正(N2)=3v逆(H2) |
查看答案和解析>>
科目: 来源:2012届福建省厦门外国语学校高三上学期10月份月考化学试卷 题型:单选题
某温度下反应N2O4(g) 2NO2 (g);ΔH>0,在密闭容器中达平衡,下列说法正确的是( )
2NO2 (g);ΔH>0,在密闭容器中达平衡,下列说法正确的是( )
| A.保持体积不变,加入少许N2O4,平衡向逆反应方向移动 |
| B.升高温度v正、v逆都增大,v正增大的倍数小于v逆增大的倍数 |
| C.保持体积不变,升高温度,再达平衡时混和气体颜色变深 |
| D.达到平衡后,降低温度或减小压强平衡移动的方向一致 |
查看答案和解析>>
科目: 来源:2012届福建省厦门外国语学校高三上学期10月份月考化学试卷 题型:单选题
在一密闭容器中有如下反应:L (s) + a G (g)  b R (g) 温度和压强对该反应的影响如右图所示。
b R (g) 温度和压强对该反应的影响如右图所示。
其中压强P1 < P2,由此可判断( )
A. 正反应为放热反应
B. 化学方程式中的计量数a>b
C . G的转化率随温度升高而减小
. G的转化率随温度升高而减小
D. 增大压强,容器内气体质量不变
查看答案和解析>>
科目: 来源:2012届福建省厦门外国语学校高三上学期10月份月考化学试卷 题型:单选题
定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)="x" mol、n(H2)="y" mol、n(NH3)="z" mol (x、y、z均不为0 ),平衡时,n(N2)=0.1mol、n(H2)=0.3mol、n(NH3)=0.08mol。下列有关判断不合理的是( )
| A.x : y ="1" : 3 |
| B.N2、H2的转化率不相等 |
| C.平衡时,H2与NH3的生成速率之比为3 : 2 |
| D.x的取值范围为0<x<0.14 |
查看答案和解析>>
科目: 来源:2012届甘肃省甘谷二中高三上学期第一次检测化学试卷 题型:单选题
在一定温度下,向a L密闭容器中加入1 mol X和2mol Y,发生如下反应:X(s) + 2Y(g) 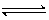 2Z(g) ,此反应达到平衡的标志是
2Z(g) ,此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内X、Y、Z的浓度之比为l : 2 : 2 |
| C.容器内各物质的浓度不随时间变化 |
| D.单位时间消耗0.1 mol X同时生成0.2 mol Z |
查看答案和解析>>
科目: 来源:2011-2012年湖南省醴陵二中、醴陵四中高二上学期期中考试化学试卷 题型:单选题
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
 2Z,其平衡常数为1600
2Z,其平衡常数为1600查看答案和解析>>
科目: 来源:2011-2012年湖南省醴陵二中、醴陵四中高二上学期期中考试化学试卷 题型:单选题
下列叙述中,不能用平衡移动原理解释的是( )
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com