
科目: 来源:2012-2013学年辽宁省盘锦市第二高级中学高二9月月考化学试卷(带解析) 题型:填空题
(9分)A和B反应生成C,该反应为可逆反应。假定反应由A、B开始,它们的起始浓度均为1 mol?L-1,反应进行2min后A的浓度为0.8 mol?L-1,B的浓度为0.6 mol?L-1,C的浓度为0.6 mol?L-1。则2min内反应的平均速率:
v(A)=____________, v(B)=_____________, v(C)=_______________,
该反应的化学反应方程式为:______________________________。
查看答案和解析>>
科目: 来源:2012-2013学年四川省双流中学高二入学考试化学试卷(带解析) 题型:填空题
( 6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
①由图中的数据分析,该反应的化学反应方程式为 ;
②反应开始至2min,Z的平均反应速率为 ;
③若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
查看答案和解析>>
科目: 来源:2011-2012学年河北省涿州铁中高二上学期期中考试化学试卷(带解析) 题型:填空题
(14分)反应3Fe(S)+4H2O====Fe3O4(s)+4H2(g),在一可变的容积的密闭容器中进行,试回答:
(1)增加Fe的量,其正反应速率的变化是 (填增大、不变、减小,以下相同)
(2)将容器的体积缩小一半,其正反应速率 ,逆反应速率 。
(3)保持体积不变,充入N2使体系压强增大,其正反应速率 ,逆反应速率 。
(4)保持压强不变,充入N2使容器的体积增大,其正反应速率 逆反应速率 。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省温州四中高一下学期期中考试化学试卷(带解析) 题型:填空题
(8分)为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50 mL密度为1.1g?cm-3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如右图所示。请依图回答下列问题: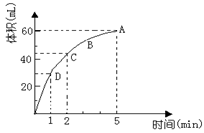
(1)实验时放出气体的总体积为 ___ ;
(2)放出一半气体所需要的时间为 ______ ;
(3)ABCD四点化学反应速率的由快到慢顺序为 ___________ ;
(4)在5min后,收集到的气体体积不再增加,原因是 。
查看答案和解析>>
科目: 来源:2012届河北省石家庄市高三第二次模拟理科综合化学试卷(带解析) 题型:填空题
(14分)氨是重要的化工产品之一,研究合成氨反应具有重要意义。
(1) 已知断裂下列化学键需要吸收的能量分别为:
 ,写出以N2(g)和H2(g)为原料合成NH3(g)的热化学方程式_______________
,写出以N2(g)和H2(g)为原料合成NH3(g)的热化学方程式_______________
(2) 某小组研究了其他条件不变时,改变某一条件对上述反应的影响,实验结果如下图所示:
①t1时刻改变的条件为__________________
②t2时刻,恒压充入氦气,t3时刻达到平衡。在图中画出t2时刻后的速率变化图像。
(3) 相同温度下,A、B、C三个密闭容器,A、B恒容,C带有可自由移动的活塞K,各向其中充人如图所示反应物,初始时控制活塞K,使三者体积相等,一段时间后均达到平衡。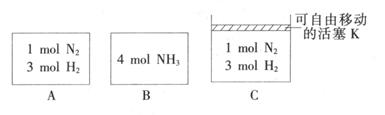
①达到平衡时,A、C两个容器中NH3的浓度分别为cl、c2,则c1______c2(填“>”、“<”或“=”)。
②达到平衡时,若A、B两容器中反应物的转化率分别为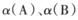 ,则
,则 ______1(填“ >”、“<”或“=”)。
______1(填“ >”、“<”或“=”)。
③达到平衡时,若容器C的体积是起始时的 ,则平衡时容器C中H2的体积分数为_______
,则平衡时容器C中H2的体积分数为_______
(4) 直接供氨式碱性燃料电池(DAFC),以KOH溶液为电解质溶液,其电池反应为 4NH3+3O2=2N2+6H2O,则负极的电极反应式为__________________。
查看答案和解析>>
科目: 来源:2011-2012学年海南省海南中学高二上学期期末考试理科化学试卷(带解析) 题型:填空题
(11分)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO3-+5SO32- +2H+= I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:[来源:学&科&网]
| | 0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1 Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度 /℃ | 溶液出现蓝色时所需时间/s |
| 实验1 | 5 | V1 | 35 | 25 | t 1 |
| 实验2 | 5 | 5 | 40 | 25 | t 2 |
| 实验3 | 5 | 5 | V2 | 0 | t 3[来源:学科网] |
查看答案和解析>>
科目: 来源:2011-2012学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(带解析) 题型:填空题
(4分)在一定温度下将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白。
(1)用D表示的平均反应速率为______。
(2) 若开始时只加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡相等,则还应加入_____ mol B物质。
查看答案和解析>>
科目: 来源:2011-2012学年福建省福州文博中学高一下学期期中考试化学试卷(带解析) 题型:填空题
(6分)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如下图所示,分析判断:________段化学反应速率最快,_____段收集的二氧化碳气体最多。
(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 |
查看答案和解析>>
科目: 来源:2011-2012学年浙江省宁波市八校高一下学期期末联考化学试卷(带解析) 题型:填空题
(5分)随着世界粮食需求量的增长,农业对化学肥料的需求量越来越大,其中氮肥是需求量最大的一种化肥。而氨的合成为氮肥的生产工业奠定了基础,其原理为:N2+3H2 2NH3
2NH3
(1)在N2+3H2 2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为 ;
2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol·L-1。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为 ;
A.2 s B.3 s C.4 s D.6 s
(2)下列4个数据是在不同条件下测得的合成氨反应的速率,其中反应最快的是 ;
A.v(H2)=0.1 mol·L-1·min-1 B.v(N2)=0.1 mol·L-1·min-1
C.v(NH3)=0.15 mol·L-1·min-1 D.v(N2)=0.002mol·L-1·min-1
(3)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是 。
2NH3(g) △H<0。下列各项能说明该反应已经达到平衡状态的是 。
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6 mol N—H键
D.反应消耗N2、H2与产生NH3的速率之比1︰3︰2
查看答案和解析>>
科目: 来源:2011-2012学年山东省汶上一中高一下学期期中考试化学试卷(带解析) 题型:填空题
(8分)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题: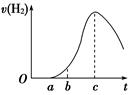
(1)曲线由O →a段不产生氢气的原因是____________________________________________________________;
有关反应的化学方程式为
__________________________________________________;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是
________________________________________________________________________
________________________________________________________________________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________;
(4)该反应若使用催化剂,可使H2产量增多吗?______(填“会”或“不会”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com