
科目: 来源:2009一2010年度吉林一中下学期高一期中考试化学卷 题型:填空题
某温度下,在一固定容积的容器中进行如下反应N2+3H2  2NH3,下列情况一定能说明反应已达到限度的是: 。(填序号)
2NH3,下列情况一定能说明反应已达到限度的是: 。(填序号)
① 容器内气压不随时间变化 ② 1个N≡N键断裂的同时,有6个N—H键断裂
③ 用N2、H2、NH3的物质的量浓度变化表示化学反应速率的比为1:3:2。
④ 容器内气体密度不再改变 ⑤ 混合气的平均相对分子质量不随时间变化
查看答案和解析>>
科目: 来源:2009一2010年度吉林一中下学期高一期中考试化学卷 题型:填空题
下表是元素周期表的一部分:
| I A | II A | III A | IV A | V A | VI A | VII A | ||
| 2 | ② | ③ | ④ | | ⑤ | ⑥ | | ||
| 3 | ⑦ | ⑧ | ⑨ | | ⑩ | 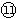 | 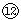 |
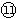 的氢化物的还原性______稳定性 (填强或弱)
的氢化物的还原性______稳定性 (填强或弱)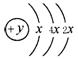 ,在周期表位于 。该
,在周期表位于 。该 与⑧形成化合物形成过程: 。
与⑧形成化合物形成过程: 。 的最高价氧化物对应水化物反应的离子方程式:
的最高价氧化物对应水化物反应的离子方程式: 。
。查看答案和解析>>
科目: 来源:2010届安庆市高考模拟试题理综化学部分(二) 题型:填空题
某条件下,在2 L密闭容器中发生如下反应2NO2(g) 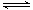 2NO(g)+O2(g)
2NO(g)+O2(g)
在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
在2L密闭容器内,800℃时反应:2NO2(g) 2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表: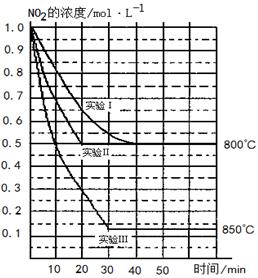
⑴实验Ⅱ隐含的反应条件是
⑵写出该反应的平衡常数表达式: K= 。
该反应是________(填“吸” 或“ 放”)热反应。
⑶若实验Ⅰ中达平衡后,再向密闭容器中通入2 mol由物质的量之比为1:1组成的NO2与O2混合气体(保持温度不变),则平衡将 移动。
⑷若将上述第⑶题所得的平衡混和气体通入足量的NaOH溶液中,使气体被完全吸收。
生成的产物及其物质的量为 。
⑸NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转
化为无害的参与大气循环的物质,该反应的化学方程式为 。
(任写一个)
查看答案和解析>>
科目: 来源:2010届河北沙河一中考前热身理综化学卷(二) 题型:填空题
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
(1)某温度下,2SO2(g)+ O2(g)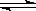 2SO3(g);△H=mkJ·mol-1
2SO3(g);△H=mkJ·mol-1
K的大小与温度(T)的关系如右图中曲线所示,则m 0(填“>”“=”或“<”);
b点时v(正) v(逆)(填“<”、“>”或“=”)。反应的焓变(△H)将 (填“增大”、“减小”或“不变”)。
(2)若反应物起始的物质的量相同,下列关系图错误的是________ (填序号)。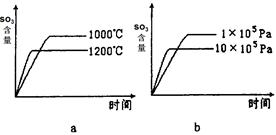
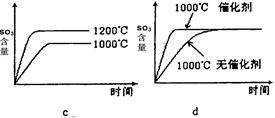
(3)某硫酸厂利用S02尾气、废铁屑、空气、水合成绿矾(FeS04·7H20),反应中作还原剂的物质是 。
(4)将反应后的混合气体用氨水吸收可得到 (NH4)2SO3和(NH4)2SO4两种化工原料
①对于(NH4)2SO3溶液,某同学写出了如下的正确关系式:
2[c(SO32-)+c(HSO3-)+c(H2SO3)]=c(NH4+)+c(NH3·H2O)
请分析该同学的依据是
②在(NH4)2SO4溶液中存在:NH4++H2O NH3·H2O+H+,则该反应常温下的平衡常数K= (已知:常温下,
NH3·H2O+H+,则该反应常温下的平衡常数K= (已知:常温下,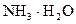 的电离平衡常数Kb=1.7×10—5 mol·L—1)
的电离平衡常数Kb=1.7×10—5 mol·L—1)
(5)三氧化硫吸收后所得的硫酸常用来制备BaSO4作X射线透视时的内服造影剂,胃酸很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释) 。万一误服了少量BaCO3,应尽快用大量0.5mol/LNa2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为 mol/L(己知25℃时,Ksp(BaSO4)=l×10-10,Ksp(BaCO3)=1×l0-9)。
查看答案和解析>>
科目: 来源:2009—2010学年河北冀州中学高一下学期期中考试化学卷 题型:填空题
在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定温度,一定压强下,发生如下反应:2H2(g)+CO(g)  CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,以H2的浓度变化表示的该反应的速率 ;平衡混合气的密度与相同状况下的氢气密度之比 。
CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,以H2的浓度变化表示的该反应的速率 ;平衡混合气的密度与相同状况下的氢气密度之比 。
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题十四 化学计算 题型:填空题
(8分)高炉炼铁过程中发生的主要反应为 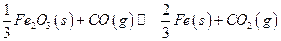
已知该反应在不同温度下的平衡 常数如下:
常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(C02)= _____ ________、CO的平衡转化率= _____________:
________、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
| A.减少Fe的量 | B.增加Fe203的量 | C.移出部分C02 |
| D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂 |
查看答案和解析>>
科目: 来源:2010年高考化学试题分项专题十四 化学计算 题型:填空题
(16分)硼酸(H3BO3)在食品、医药领域应用广泛。
(1)请完成B2H6气体与水反应的化学方程式:B2H6 + 6H2O=2H3BO3 +________。
(2)在其他条件相同时,反应H3BO3 +3CH3OH B(OCH3)3 +3H2O中,H3BO 3的转化率(
B(OCH3)3 +3H2O中,H3BO 3的转化率( )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
①温度对应该反应的反应速率和平衡移动的影响是____ ___
②该反应的 _____0(填“<”、“=”或“>”).
_____0(填“<”、“=”或“>”).
(3)H3BO 3溶液中存在如下反应:
H3BO 3(aq)+H2O(l) [B(O
[B(O H)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)="2." 0 × 10-5mol·L-1,c平衡(H3BO 3)≈c起始(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
H)4]-( aq)+H+(aq)已知0.70 mol·L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)="2." 0 × 10-5mol·L-1,c平衡(H3BO 3)≈c起始(H3BO 3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
查看答案和解析>>
科目: 来源:2010年普通高等学校招生统一考试理综试题化学部分(全国卷II) 题型:填空题
(5分)
向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应;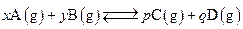
已知:平均反应速率 ;反应2min时,A的浓度减少了
;反应2min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有amolD生成。
mol,有amolD生成。
回答下列问题:
(1)反应2min内, =,
=,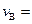 ;
;
(2)化学方程式中, 、
、 、
、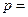 、
、 ;
;
(3)反应平衡时,D为2amol,则B的转化率为;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5amol,则该反应的
0;(填“>”、“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
①反应速率(填“增大”、“减小”或“不变”),理由是;
②平衡时反应物的转化率(填“增大”、“减小”或“不变”),理由是;
查看答案和解析>>
科目: 来源:2010年福建省厦门外国语学校高三模拟考试(理综)化学部分 题型:填空题
(16分)应用化学反应需要研究化学反应的条件、限度和速率。
(1)已知反应:Br2+2Fe2+=2Br-+2Fe3+,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反应后,溶液中除含有Cl-外,还一定有 (填序号)。
①含Fe2+,不含Fe3+②含Fe3+,不含Br-③含Fe3+,还含有Br-
(2)773 K、固定体积的容器中,反应CO(g)+2H2(g) CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。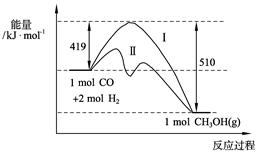
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为 ;
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可) 、 ;
③下列与催化剂有关的说法中,正确的是 (填字母序号)。
a. 使用催化剂,使反应CO(g)+2H2(g) CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1
b. 使用催化剂, 能够提高反应物转化率
c. 使用催化剂,不能改变反应的平衡常数K
(3)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。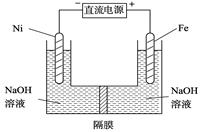
① Ni作 (填“阴”或“阳”) 极;
②Ni电极的电极反应式为: 。
。
(4)氧化还原反应中实际上包含氧化和还原两个过程。下面是HNO3发生的一个还原过程的反应式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五种物质中的 (填化学式)能使上述还原过程发生。
②欲用下图装置通过测定气体生成量测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定 推(计)算反应速率。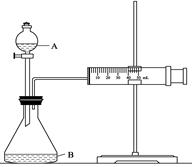
查看答案和解析>>
科目: 来源:2010年上海市金山中学高一第二学期阶段质量检测化学试题 题型:填空题
在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如下图,据图回答下列问题: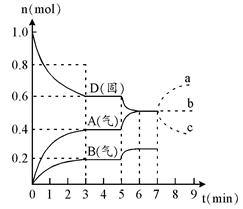
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为 。
(2)根据右图写出该反应的化学方程式 。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如右图,则该反应是 (填“放热”或“吸热”)反应。若在第7分钟时增加D的物质的量,A的物质的量变化正确的是_____(用图中a~c的编号回答)
(4)某同学在学习了“化学反应速率和化学平衡”专题后,发表如下观点,你认为错误的是 。
a.化学反应速率理论是研究怎样在一定时间内快出产品
b.化学反应速率理论是研究怎样提高原料转化率
c.化学平衡理论是研究怎样使用有限原料多出产品
d.正确利用化学反应速率和化学平衡理论都可以提高化工生产的综合效益
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com