
科目: 来源:2011届安徽省合肥市高三第一次教学质检化学试卷 题型:填空题
(12分)
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为: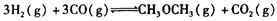

它可以分为两步,反应分别如下:

 :__________________ ______________
:__________________ ______________
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速和CO的转化率的是_______(填字母代号)。
a.降低温度 b.加人催化剂 c.缩小容器体积
d.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入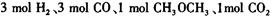 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率 的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
②平衡时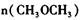 =_________________,平衡时CO的转化率= _________________。
=_________________,平衡时CO的转化率= _________________。
查看答案和解析>>
科目: 来源:2011届广东省揭阳一中高三学年会考(理综)化学部分 题型:填空题
(16分)氨气是一种重要的基础化工原料,用途广泛。
(1)在微电子工业中,氨水可作刻蚀剂H2O2的清除剂,产物不污染环境。该反应的化学方程式为2NH3 + 3H2O2= +6H2O
(2)工业中常用以下反应合成氨:N2+3H2 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。
该反应平衡常数的数学表达式为 ;实验②平衡时H2的转化率为_____ 。
(3)据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:_______ 理由: ________
③条件:_______ 理由: ________
查看答案和解析>>
科目: 来源:2011届浙江省台州市高三上学期期末考试化学试卷 题型:填空题
(14分)痛风是关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
① HUr(尿酸,aq)  Ur-(尿酸根,aq) + H+(aq) (37℃时,Ka =4.0×10-6)
Ur-(尿酸根,aq) + H+(aq) (37℃时,Ka =4.0×10-6)
②NaUr(s)  Ur-(aq) + Na+(aq)
Ur-(aq) + Na+(aq)
(1)37℃时,0.5 L水中可溶解4.0×10-3 mol尿酸钠,此温度下尿酸钠的Ksp为 ▲ 。
(2)关节炎发作大都在脚趾和手指的关节处,这说明温度降低时,反应②的Ksp ▲ (填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是 ▲ (填“放热”或“吸热”)反应。
(3)37℃时,某病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3 mol·L-1,其中尿酸分子的浓度为4.0×10-4 mol·L-1,该病人尿液的pH为 ▲ 。
(4)常温下,将0.2 mol·L-1的HUr溶液和0.1 mol·L-1 NaOH溶液等体积混合,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是 ▲ 。
| A.c(HUr) > c(Ur-) | B.pH > 7 |
| C.c(Na+)=c(HUr)+c(Ur-) | D.2 c(H+)=2 c(OH-)+[c(Ur-) -c(HUr)] |
查看答案和解析>>
科目: 来源:2011届江苏省宿豫中学高三第二次模拟考试化学试卷 题型:填空题
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。
⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH= ▲ 。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH= ▲ 。(用含ΔH1、ΔH2的代数式表示)
⑵CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。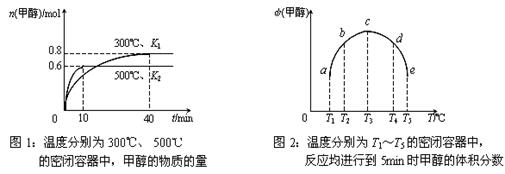
①该反应的ΔH3 ▲ 0(选填“<”、“>”或“=”,下同),K1 ▲ K2。
②将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有 ▲ 。
⑶某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式: ▲ 。
查看答案和解析>>
科目: 来源:2011届宁夏银川一中高三第一次模拟考试(理综)化学部分 题型:填空题
(14分)
工业合成氨反应:N2+3H2 2NH3,在一定条件下已达到平衡状态。
2NH3,在一定条件下已达到平衡状态。
(1)若降低温度,会使上述平衡向生成氨的方向移动,生成每摩尔氨的反应热数值是46.2KJ/mol,则该反应的热化学方程式为 。
(2)若在恒温条件下,将N2与H2按一定比例混合的气体通入一个容积为2升固定容积的密闭容器中,5分钟后反应达平衡时,n(N2)="1.2mol," n(H2)="1.2mol," n (NH3)=0.8mol,则反应速率V(N2)= mol·L-1·min-1,H2的转化率= ,平衡常数= 。若保持容器的温度和容积不变,将上述平衡体系中的混合气体的浓度增大1倍,则平衡 (填向左﹑向右或不移动)移动。
(3)若在恒温恒压条件下,将1 molN2与3 molH2的混合气体通入一个容积可变的容器中发生反应,达平衡后,生成a molNH3,这时N2的物质的量为 mol,(用含a的代数式表示);若开始时只通入N2与H2,达平衡时生成3amolNH3,则开始时应通入N2 3mol,H2 = mol(平衡时NH3的质量分数与前者相同);若开始时通入x molN2﹑6molH2和2mol NH3,达平衡后,N2和NH3的物质的量分别为y mol和3a mol,则x= mol,y= mol(用含a的代数式表示)
查看答案和解析>>
科目: 来源:2011届广东省执信中学高三2月月考理综化学部分 题型:填空题
已知 :N2(g)+3H2(g)  2NH3(g) ΔH=-92 kJ·mol-1。
2NH3(g) ΔH=-92 kJ·mol-1。
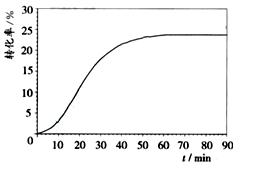
(1) 在500℃、2.02×107Pa和铁催化条件下2L密闭容器中充入1molN2和3mol H2,10 min时达到平衡,有0.2 mol NH3生成,则10 min内用氢气表示的该反应的平均速率v(H2)为 ,H2的转化率为__________。
(2)充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是
 。
。
(3)为有效提高氢气的转化率,实际生产中宜采取的措施有____________
| A.降低温度 | B.不断补充氮气 | C.恒容下充入He来增大压强 |
| D.升高温度 E.原料气不断循环 F.及时移出氨 |
查看答案和解析>>
科目: 来源:2010~2011学年湖南省常德市上学期高三检测化学试卷 题型:填空题
氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为 ;
|
 2NH3(g) △H<0,得到如下数据:
2NH3(g) △H<0,得到如下数据:| 实验组 | 温度/℃ | 起始量/mol | 2分钟/mol | 平衡常数 | |
| H2 | N2 | NH3 | |||
| 1 | 298 | 6 | 2 | 1.2 | 4.1×106 |
| 2 | 398 | 3 | 1 | 0.8 | K1 |
| A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2 |
| B.υ(N2)(正)=3υ(H2)(逆) |
| C.容器内压强保持不变 |
| D.混合气体的密度保持不变 |
查看答案和解析>>
科目: 来源:2011届广东省深圳市高三第一次调研考试(理综)化学部分 题型:填空题
Ⅰ.已知溶液导电性与其中离子浓度有定量关系。某兴趣小组设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是________________(填序号)
Ⅱ.Fe2+、SO32-和I-都具有还原性。为了比较其还原性强弱,进行以下探究并回答:
(1)已知:①还原性:SO32-> Fe2+;②FeSO3难溶于水。
(2)在(1)的基础上,完成下列假设。
假设1,还原性:I->SO32-> Fe2+;
假设2,还原性: SO32-> I- >Fe2+;
假设2,还原性: ______________________。
(3)实验探究:现对假设2进行探究。完成实验步骤以及预期的现象和结论。
限选以下试剂:0.1mol/L Na2SO3、0.1mol/L KI、0.1mol/L FeCl3、10%KSCN、新制饱和氯水、淀粉溶液、稀HNO3、1mol/L HCl、1mol/L BaCl2
 实验操作 实验操作 | 预期的现象及结论 |
| 步骤1:取1mL0.1mol/L Na2SO3和1mL0.1mol/L KI溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 | |
| 步骤2:____________________________ _____________________________________ | ____________________________________ _______________________________________ |
 步骤3:取1mL0.1mol/L KI和1mL0.1mol/LFeCl2溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 步骤3:取1mL0.1mol/L KI和1mL0.1mol/LFeCl2溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 | |
| 步骤4:____________________________ _____________________________________ | ____________________________________ _______________________________________ |
查看答案和解析>>
科目: 来源:2010-2011学年湖北省武汉市三角路中学高二上学期期末考试化学试卷 题型:填空题
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g)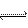 CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。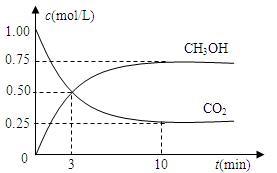
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1 mol CO2和4 mol H2 |
 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。查看答案和解析>>
科目: 来源:2011届陕西省西安市五大名校高三第一次模拟考试理综化学部分 题型:填空题
( 14分)在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g) + Y(g) a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)
a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则:
(1)化学计量数a的值为 。
(2)写出该反应平衡常数K的表达式  (a必须用具体的值表示)。
(a必须用具体的值表示)。
(3)下列说法中能说明该反应达到了化学平衡状态的是 。
A.容器内压强一定 B.容器内气体的密度一定
C.容器内Z分子数一定 D.容器内气体的质量一定
(4)X的转化率α= ,Y的平衡浓度为 。(均用含Q、Q1的代数式表示)
(5)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是 (稀有气体不参与反应)。
A.2 molX、1mol Y、1molAr
B.a molZ、1mol W
C.1 molX、0.5mol Y、0.5a molZ、0.5 mol W
D.2 molX、1mol Y、1molZ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com