
科目: 来源:2011-2012学年广东省始兴县风度中学高一下学期期末考试理综化学卷(带解析) 题型:填空题
(16分)Ⅰ.依据氧化还原反应:2Ag+(aq)+Cu(s) ===Cu2+(aq) +2Ag(s)设计原电池,请回答下列问题:
(1)负极材料是____________;电解质溶液是____________;
(2)正极发生的电极反应为________________________;
(3)电解质溶液中Ag+向_________极移动。
Ⅱ.一定温度下在某定容容器中发生反应:2A(g) +3B(g) ===2C(g),开始时,A的浓度为2 mol·L -1,B的浓度是4 mol·L-1,2 min后,A的浓度减少0.8 mol·L-1,则
(1)v(B) =___________,v(C) =____________。
(2)在2min末,C的浓度是____________,B的浓度是____________。
查看答案和解析>>
科目: 来源:2011-2012学年黑龙江省庆安三中高一下学期期末考试化学试卷(带解析) 题型:填空题
(1)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
①该反应的化学方程式: ;
②反应开始至2min末,X的反应速率为 (mol·L-1·min-1);
③3min后图中曲线所表示的含义是 。
(2)(4分)下图为石油蒸馏的装置图,根据此图回答下列问题。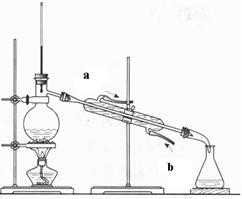
①温度计的水银球插在什么位置?
②蒸馏烧瓶中除了加入石油外还要加入什么?
③冷却水的流动方向如何?(填A或B,下题同)
A、a→b B、 b→a
④得到的汽油、煤油是纯净物吗?
A、是 B、不是
查看答案和解析>>
科目: 来源:2012届福建省芗城三校高三下学期第二次考试化学试卷(带解析) 题型:填空题
(共10分)
(1)已知可逆反应:M(g)+N(g)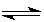 P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:
①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。
| A.加入一定量M | B.加入一定量N |
| C.反应温度升高 | D.缩小容器体积 |
查看答案和解析>>
科目: 来源:2011-2012学年内蒙古包头33中高一下学期期末考试化学试卷(带解析) 题型:填空题
(8分) t℃时,将 2molSO2和 1molO2通入体积为 2L 的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成 SO3 的平均反应速率为 ;平衡时,SO2 转化率为 .
(2)下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化 D.相同时间内消耗 2nmolSO2的同时消耗 nmolO2
E.相同时间内消耗 2nmolSO2 的同时生成 nmolO2 F.混合气体密度不再变化
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
查看答案和解析>>
科目: 来源:2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(带解析) 题型:填空题
(10分). 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)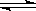 CH3OH(g)
CH3OH(g)
根据题意完成下列各题: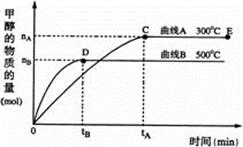
(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
| A.氢气的浓度减少 | B.正反应速率加快,逆反应速率也加快 |
| C.甲醇的物质的量增加 | D.重新平衡时n(H2)/n(CH3OH)增大 |
查看答案和解析>>
科目: 来源:2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(带解析) 题型:填空题
(9分)在一定温度下,向一个容积不变的容器中加入3 mol SO2和2 mol O2及固体催化剂,发生反应:2SO2(g)+O2(g)=2SO3(g)ΔH=-196.6 kJ/mol,平衡时容器内气体压强为起始时的90%。
(1)加入3mol SO2和3mol O2发生反应,达到平衡时,SO2的转化率为_____。
(2)保持温度不变,在相同的容器中,将起始物质的物质的量改为a mol SO2、b mol O2、c mol SO3(g)(c>0),欲使平衡时SO3的体积分数为2/9,O2的体积分数为3/9,则:
①达到平衡时,(1)与(2)放出的热量________(填序号)。
| A.相等 | B.前者小于后者 | C.前者大于后者 | D.无法确定 |
查看答案和解析>>
科目: 来源:2011-2012学年陕西省师大附中高一下学期期末考试化学试卷(带解析) 题型:填空题
(13分)在100℃时,将0.100 mol 的四氧化二氮气体充入 1 L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)(mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
科目: 来源:2011-2012学年河北省邢台一中高一下学期期末考试化学试卷(带解析) 题型:填空题
(8分)下表表示合成氨反应(N2+3H2 2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
 压强(MPa) 压强(MPa) 氨的含量 氨的含量温度(℃) | 0.1 | 10 | 30 | 60 | 100 |
| 200 | 0.153 | 0.815 | 0.899 | 0.954 | 0.988 |
| 300 | 0.022 | 0.520 | 0.710 | 0.842 | 0.926 |
| 400 | 0.004 | 0.251 | 0.470 | 0.652 | 0.798 |
 欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:
欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为: 查看答案和解析>>
科目: 来源:2011-2012学年云南大理州宾川县第四高级中学高二4月月考化学试卷(带解析) 题型:填空题
(8分)现有反应aA(g)+bB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的正反应是________热反应,且a+b________p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同),正反应速率________。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比 将________。
将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
查看答案和解析>>
科目: 来源:2011-2012学年广东省湛江一中高一6月月考理科综合化学试卷(带解析) 题型:填空题
(16分)某温度时,在2L容器中X、Y、Z三种气体物质的量随时间的变化关系曲线如图(2)所示。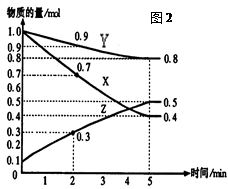
(1)由图中的数据分析,该反应的化学方程式为 。
(2)反应开始至5min,Z的平均反应速率为 ;
(3)反应开始至5min ,正反应速率逐渐 ;逆反应速率逐渐 , 5min后Z的物质的量不再改变,原因是下列的 ;
A.正逆反应都停止了
B.正反应速率为零
C.正逆反应速率相等,反应达到平衡状态
D.逆反应速率为零
(4)下列措施能使正反应速率增大的是
A.升高温度 B.降低温度
C.增大Y的浓度 D.减少Z的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com