
科目: 来源:2013届山西省高新二中高考一轮复习阶段考试化学试卷(带解析) 题型:填空题
如图Ⅰ,在恒压密闭容器M中加入2 mol A和2 mol B,起始时容器体积为V L,发生如下反应并达到化学平衡状态:2 A(?)+B(?) x C(g);ΔH<0
x C(g);ΔH<0
平衡时A、B、C的物质的量之比为1∶3∶4,C的物质的量为 y mol。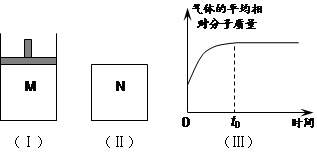
⑴根据题中数据计算,x =_________、y =_________;
⑵如图Ⅱ,在体积为V L的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡),平衡时容器中C的物质的量为z mol。由于反应物A、B的状态未知,则z和y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
| 可能的情形 | A、B是否为气态 | z与y的大小关系 | M(B)与M(C)的大小关系 (M表示摩尔质量) | |
| A | B | |||
| ① | 是 | 不是 | z =y | 不确定 |
| ② | | | | |
| ③ | | | | |
查看答案和解析>>
科目: 来源:2011-2012学年云南省昆明三中高二下学期期末考试化学试卷(带解析) 题型:填空题
(13分)在某一容积为2 L的密闭容器内,加入0.8 mol的H2和0.6 mol的I2,在一定条件下发生如下反应: H2(g) + I2(g) 2HI(g) △H = Q(Q<0)反应中各物质的浓度随时间变化情况如图1
2HI(g) △H = Q(Q<0)反应中各物质的浓度随时间变化情况如图1
(1)根据图1数据,反应开始至达到平衡时,平均速度v(HI)为 。
(2)反应达到平衡后,第8分钟时:①该反应的平衡常数表达式:K = ;若升高温度,化学平衡常数K (填“增大”、“减小”或“不变”),HI浓度的变化正确的是 (用图2中a ~ c的编号回答)。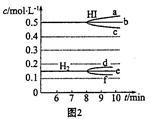
② 若加入I2,H2浓度的变化正确的是 (用图2中d ~ f的编号回答)。
(3)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍, 请在图3中画出8分钟后HI浓度的变化情况。
查看答案和解析>>
科目: 来源:2011-2012学年云南省昆明三中高一下学期期末考试化学试卷(带解析) 题型:填空题
(4分)在一定温度下,固定容积的2L容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图所示:
(1)____________时(填t1、t2或者t3),正、逆反应速率相等,化学反应达到了平衡状态。
(2)该反应的化学方程式为_____________________。
查看答案和解析>>
科目: 来源:2011-2012学年云南省昆明三中高一下学期期末考试化学试卷(带解析) 题型:填空题
(14分)已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
请回答下列问题:
(1)写出A的电子式
B、D分子中的官能团名称分别是 、 。
(2)写出下列反应的化学方程式,并注明反应类型:
① ;反应类型: ;
② ;
④ ;反应类型: ;
(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的是(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④生成物中乙酸乙酯的物质的量不再变化
查看答案和解析>>
科目: 来源:2013届辽宁省五校协作体高三上学期期初联考化学试卷(带解析) 题型:填空题
(14分)
(1)某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。已知:
N2(g)+2O2(g)=2NO2(g) △H1=+68kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l) △H2=-534kJ/mol
请写出该次发射火箭时燃烧反应的热化学方程式 。
(2)下表是不同温度下水的离子积数据:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
 5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。
5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。 N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。
N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。查看答案和解析>>
科目: 来源:2012-2013学年山西省太原五中高二8月月考化学试卷(带解析) 题型:填空题
在某一容积为2L的密闭容器内,加入0.8 mol 的H2和0.6 mol 的I2 ;在一定的条件下发生如下反应:H2(g) + I2(g) 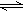 2HI(g) + Q(Q>0)。反应中各物质的浓度随时间变化情况如图1:
2HI(g) + Q(Q>0)。反应中各物质的浓度随时间变化情况如图1:
⑴根据图1数据,反应开始至达到平衡时,平均速率V(HI)为___________。(精确到小数点后第3位)
⑵反应达到平衡后,第8分钟时,若升高温度, HI浓度的变化正确的是___________(用图2中a~c的编号回答)。
⑶反应达到平衡后,第8分钟时,若加入I2, 则H2浓度的变化正确的是___________(用图2中d-f的编号回答)。
⑷反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图中画出从第8分钟开始向后HI浓度的变化情况。
查看答案和解析>>
科目: 来源:2012-2013学年山西省太原五中高二8月月考化学试卷(带解析) 题型:填空题
在水溶液中呈橙红色的Cr2O72-与呈黄色的CrO42-有下列平衡关系:Cr2O72-+H2O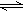 2CrO42-+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
2CrO42-+2H+,把重铬酸钾(K2Cr2O7)溶于水配成稀溶液呈橙色。
(1)取少许上述溶液加入NaOH溶液,溶液变_________色,因为___ ________。
⑵向⑴中再加入过量稀H2SO4,则溶液呈__ __色,因为__________ _________。
⑶取少许原溶液,向其中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡_____ ____,溶液颜色将_____ ____。
查看答案和解析>>
科目: 来源:2012-2013学年山西省太原五中高二8月月考化学试卷(带解析) 题型:填空题
合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气中的CO,其反应是:
[Cu(NH3)2Ac]+CO+NH3 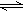 [Cu(NH3)3] Ac·CO;(△H<0)
[Cu(NH3)3] Ac·CO;(△H<0)
⑴醋酸二氨合铜(I)吸收CO的生产适宜条件是 ;
⑵吸收CO后的醋酸铜氨液经过适当处理又可再生,恢复其吸收CO的能力以供循环使用,醋酸铜氨液再生的适宜条件是___________________________________。
查看答案和解析>>
科目: 来源:2012-2013学年山西省太原五中高二8月月考化学试卷(带解析) 题型:填空题
在一定温度和压强下,将N2和H2按1:3的体积比混合进入密闭容器内反应,达平衡后(温度,压强不变)氨占总体积的20%,则H2占总体积的____________。混合气体的平均相对分子质量为___________。
查看答案和解析>>
科目: 来源:2013届江西省吉安一中、新余一中高三联考化学试卷(带解析) 题型:填空题
(6分)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g) + CO(g)  CH3OH(g) △H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g) △H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com