
科目: 来源:2013届河北省石家庄市第二实验中学高二上学期期中考试理科化学试卷(带解析) 题型:填空题
在2L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

查看答案和解析>>
科目: 来源:2013届河北省石家庄市第二实验中学高二上学期期中考试理科化学试卷(带解析) 题型:填空题
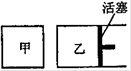
如下图所示,在容器A中装有20℃的水50 mL,容器B中装有1 mol/L的盐酸50 mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2(g)  N2O4(g) ΔH=-57 kJ/mol,
N2O4(g) ΔH=-57 kJ/mol,
当向A中加入50 gNH4NO3晶体使之溶解;向B中加入2 g苛性钠时:
C中的气体颜色__________,D中的气体颜色__________(填“变浅”或“变深”)。
请简述原因 。
(2)若25℃时,起始时仅有NO2气体,反应2NO2 N2O4达到平衡时,c(NO2)=0.0125 mol/L,c(N2O4)=0.0321 mol/L,则NO2的起始浓度为__________,NO2的转化率为__________。
N2O4达到平衡时,c(NO2)=0.0125 mol/L,c(N2O4)=0.0321 mol/L,则NO2的起始浓度为__________,NO2的转化率为__________。
查看答案和解析>>
科目: 来源:2012-2013学年北京市第六十六中学高一下学期期中考试化学试卷(带解析) 题型:填空题
在一密闭的2 L容器中装有4 mol SO2和2 mol O2,在一定条件下开始反应。2 min末测得容器中有1.6 mol SO2,请计算:(1)2 min末SO3的浓度 ;(2)2 min内SO2的平均反应速率 (3)2 min末SO2与O2的压强的比 。
查看答案和解析>>
科目: 来源:2012-2013学年江苏省宿迁青华中学高二下学期期中考化学普通班试卷(带解析) 题型:填空题
已知A(g)+B(g)  C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
(1)该反应是_______反应(填“吸热”、“放热”)。当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),
(2)在反应体系中加入催化剂,反应速率增大,E的变化是_________,(填“增大”、“减小”或“不变”) E的大小对该反应的反应热有无影响? 。
查看答案和解析>>
科目: 来源:2012-2013学年江苏省宿迁青华中学高二下学期期中考化学普通班试卷(带解析) 题型:填空题
高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO (g)  Fe(s)+ CO2(g) △H>0
Fe(s)+ CO2(g) △H>0
(1)此反应的平衡常数表达式为:K=
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比 (填“增大”、“减小”或“不变”)。
(3)已知1100℃时,K= 0.263。某时刻测得高炉中c(CO2)=" 0.025" mol·L-1,c(CO)=" 0.1" mol·L-1,在这种情况下,该反应 (填“向正反应方向进行”或“向逆反应方向进行”或“处于化学平衡状态”)。
(4)由氢气和氧气反应生成1mol水蒸气放热241.8KJ,已知氢气中H-H键能为436 kJ/mol,氧气分子中 O=O键能为498 kJ/mol,则水分子中O-H键的键能为 kJ/mol 。若1 g水蒸气转化成液态水时放热2.5 kJ,则反应H2(g) + 1/2O2(g) == H2O(l)的\
△H= kJ/mol
查看答案和解析>>
科目: 来源:2012-2013学年江苏省东台市唐洋中学高二下学期期中考试化学试卷(带解析) 题型:填空题
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe2O3。
(1)将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g)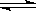 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率 、 。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率 、 。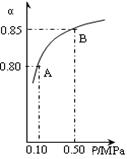
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 (填字母序号,多选倒扣分)。
A.升高温度 B.降低温度
C.增大压强 D.加入催化剂
E.移出氧气
(3)某温度下,上述反应中SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。判断:平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”)。
查看答案和解析>>
科目: 来源:2012-2013学年江苏省东台市唐洋中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(1)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 ;加入石膏(CaSO4 2H2O)可以使土壤碱性降低,有关反应的化学方程式为 。
2H2O)可以使土壤碱性降低,有关反应的化学方程式为 。
(2)在一定条件下进行如下反应:aX(g)+bY(g)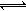 cZ(g)
cZ(g)
右图是不同温度下反应达到平衡时,反应混合物中Z的体积分数 和压强关系示意图。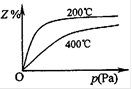
① 写出该反应的化学平衡常数表达式:K= 。随着温 度的升高,K值 (填“增大”、“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明 (字母填序号)。
| A.X的转化率越高 | B.反应进行得越完全 |
| C.达到平衡时X的浓度越大 | D.化学反应速率越快 |
查看答案和解析>>
科目: 来源:2012-2013学年江苏省南京三中高二下学期期中考试化学试卷(带解析) 题型:填空题
在一定条件下,二氧化硫和氧气发生 如下反应:
2SO2(g)+ O2 (g) 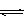 2SO3(g) (△H< 0)
2SO3(g) (△H< 0)
(1)降低温度,二氧化硫转化率_________,化学反应速率_ (以上均填增大、减小或不变)
(2)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间____ 。
(3)据图判断,反应进行至20min时,曲线发生变化的原因是__ ___(用文字表达)
(4)10min到15min的曲线变化的原因可能是 __________________(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
科目: 来源:2013届山西省忻州市高三第一次联考化学试卷(带解析) 题型:填空题
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) 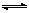 CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4 mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4 mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
请回答下列问题:
(1)在“图1”中,曲线________(填:a或b)表示使用了催化剂;该反应属于________(填:吸热、放热)反应。
(2)下列说法正确的是________。
| A.起始充入的CO为1 mol |
| B.增加CO浓度,CO的转化率增大 |
| C.容器中压强恒定时,反应已达平衡状态 |
| D.保持温度和密闭容器容积不变,再充入1 mol CO和2 mol H2,再次达到平衡时n(CH3OH)/n(CO)会减小 |
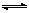 CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数________(填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数________(填“增大”、“减小”或“不变”)。 O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol查看答案和解析>>
科目: 来源:2012-2013学年上海市七校高一5月阶段检测化学试卷(带解析) 题型:填空题
在一容积为2 L的密闭容器中,高温下发生下列反应:C(s)+H2O(g)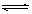 CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如右图所示:
CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如右图所示:
(1)反应处于平衡状态的时间区间是_____________。
(2)若反应进行到2 min时,改变了温度,使曲线发生如右图所示的变化,则温度为______(选填“升高”或“降低”),逆反应是____________(选填“吸”或“放”)热反应。
(3)反应至5 min时,若也只改变了某一个条件,使曲线发生如图所示变化,该条件可能是下述中的_________________。
| A.增加了C | B.增加了水蒸气 | C.降低了温度 | D.增加了压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com