
科目: 来源:2011-2012学年山东济宁梁山二中高二12月月考化学试卷 题型:单选题
将a moL/L的Na2CO3溶液与b mol/L的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断不正确的是( )
| A.c(Na+)+c(H+)>c(CO32-)+c(HCO3-)+c(OH-) |
| B.c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b |
| D.若c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3),则可确定a=b |
查看答案和解析>>
科目: 来源:2011-2012学年广东省汕头市金山中学高二12月月考化学试卷 题型:单选题
已知25℃时有关
弱酸的电离平衡常数:则下列有关说法正确的是
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃ ) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0 -11 |
查看答案和解析>>
科目: 来源:2012届沈阳铁路实验中学高三上学期第三次月考化学试卷 题型:单选题
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH 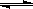 CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
| A.加入少量NaOH固体,平衡向逆反应方向移动 |
| B.升高温度,平衡向正反应方向移动 |
| C.加入水,CH3COOH的电离程度变大,溶液中c(H+)一定增大 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
查看答案和解析>>
科目: 来源:2012届河南省信阳高中高三第三次大考化学试卷 题型:单选题
下列说法正确的是:
| A.将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到Al2O3、Na2SO3 |
| B.在溶液的稀释过程中,离子浓度有的可能增大,有的可能减小,有的可能不变 |
| C.0.1 mol/L CH3COOH溶液在稀释过程中将变小 |
| D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
查看答案和解析>>
科目: 来源:2011-2012学年山东省济宁市邹城二中高二上学期期中质量检测化学试卷 题型:单选题
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是( )
| A.白色沉淀为ZnS,黑色沉淀为CuS | B.上述现象说明ZnS的Ksp小于CuS的Ksp |
| C.利用该原理可实现一种沉淀转化为更难溶的沉淀 | D.该过程破坏了ZnS的溶解平衡 |
查看答案和解析>>
科目: 来源:2011-2012学年江西省兴国县将军中学高二上学期期中考试化学试卷 题型:单选题
下列图像能正确反映所对应实验的是 
| A.①为向pH=13的NaOH溶液中不断加水 |
B. ②为向MnO2中加入一定量的H2O2溶液 ②为向MnO2中加入一定量的H2O2溶液 |
| C.③为向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
| D.④为将氨气通入醋酸溶液中 |
查看答案和解析>>
科目: 来源:2012届河北省正定中学高三第三次考试化学试卷 题型:单选题
某学习小组根据化学知识和下表的数据,设计了表中的实验,以验证酸性:盐酸>碳酸>苯酚>碳酸氢根离子,其中不合理的是 ( )
| 物质 | 电离常数 | 和溶解度(25℃) |
| C6H5OH | K=1.28×10-10 | S = 9.3g/100g水 |
| H2CO3 | K1 =4.3×10-7 | |
| K2 =5.6×10-11 | |
| | 组别 | 操作 | 判断依据 |
| A | 盐酸和碳酸 | 往碳酸钙固体中滴加盐酸 | 观察有无气体产生 |
| B | 碳酸与苯酚 | 往苯酚钠饱和溶液中,通入足量CO2 | 观察溶液是否变浑浊 |
| C | 碳酸与苯酚 | 配制同物质的量浓度的碳酸钠溶液和苯酚钠溶液 | 比较溶液的pH |
| D | HCO3-与苯酚 | 在苯酚悬浊液中,加入过量的 Na2CO3溶液 | 观察悬浊液是否变澄清 |
查看答案和解析>>
科目: 来源:2011-2012学年广西桂林十八中高二上学期期中考试化学(理)试卷 题型:单选题
关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵 溶液,下列说法不正确的是
溶液,下列说法不正确的是
| A.c(NH4+):③>① |
| B.水电离出的c(H+):②>① |
| C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O) |
D. ①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+) ①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源:2011-2012学年河北省涿州二中高二上学期期中考试化学试卷 题型:单选题
25℃时,0.01 mol/L的HCl溶液中,由水电离出的H+浓度是( )
| A.1×10-7mol·L-1 | B.1×10-12mol·L-1 |
| C.1×10-2mol·L-1 | D.1×10-14m ol·L-1 ol·L-1 |
查看答案和解析>>
科目: 来源:2010-2011学年浙江省绍兴一中高二下学期期末考试化学试卷 题型:单选题
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”)。
2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”)。
(2)在25℃下,向浓度均 为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出。
为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出。
首先生成沉淀的离子方程式为 __________________
氨水过量后,生成的沉淀会部分溶解,写出溶解沉淀的离子方程式__________________________.
( 已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10- 20 )
20 )
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中
c(NH4+) = c(Cl-)。则溶液显 _____ 性(填“酸”、“碱”或“中”),请用含a的代数式表示NH3·H2O的电离常数Kb= 。
(4) 在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则v(o2)= mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,再次达到平衡后, n(SO3)的取值范围为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com