
科目: 来源:2012届湖南省湖南师大附中高三第三次月考化学试卷 题型:填空题
(8分)常温下已知pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸是 (填“强酸”或“弱酸”)
(2)0.01mol·L-1的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合所得溶液中IO—3与Na+的物质的量的关系是n(Na+) n(IO-3)(填“大于”、“小于”或“等于”)。
(3)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,此反应的还原剂是 ,该反应的离子方程式可表示为 。
查看答案和解析>>
科目: 来源:2011-2012学年吉林省松原市宁江区实验中学高二上学期12月份月考化学试卷 题型:填空题
(10分)(1)常温下,0.1 mol/L的醋酸和0.1 mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者__________后者(填“<”“>”或“=”)。
(2)写出泡沫灭火器反应原理(用离子方程式表示): 。
(3)医院里用HgCl2的稀溶液作手术刀的消毒剂。HgCl2熔融时不导电,熔点低。HgS难溶于水和稀的强酸却易溶于饱和的NaCl溶液中。试推测HgCl2是 化合物(填“离子”或“共价”),是 电解质(填“强”或“弱”)。
(4)水是一种极弱的电解质,在常温下平均每n个水分子只有1个分子发生电离,n的值是 。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省诸暨中学高二上学期期中考试化学(理)试卷 题型:填空题
25℃时,0.1mol·L-1 HA溶液pH=2,0.1mol·L-1 HB溶液pH=3。
(1)前 者大于后者的是 (多选、错选均不给分,下同);
者大于后者的是 (多选、错选均不给分,下同);
①HA、HB的电离平衡常数 ②HA、HB的电离度 ③溶液中的c(OH-)
④溶液的导电性 ⑤溶液中由水电离出的c(H+)
(2)若HA、HB溶液的pH相同、体积相等,前者小于后者的是 ;
①HA、HB物质的量浓度 ②同时加入足量的锌,开始反应时速率
③同时加入足量的锌,反应完全后生成H2的质量 ④二种酸溶液的导电能力
⑤用1mol/LNaOH溶液分别中和二种酸,消耗NaOH溶液体积
⑥将这两种溶液分别稀释10倍后溶液的pH。 (3)若中和体积为Va浓度为0.1mol·L-1 HA溶液,消耗0.1mol·L-1 NaOH溶液的体积为Vb,且Va>Vb,下列说法一定正确的是 。(提示:CH3COONa溶液呈碱性)
①混合后溶液呈中性 ②混合后溶液呈酸性  ③混合后溶液呈碱性
③混合后溶液呈碱性
④混合后溶液中的溶质为NaA ⑤混合后溶液中的溶质为NaA和HA
⑥混合后溶液中的溶质为NaA和NaOH
查看答案和解析>>
科目: 来源:2011-2012学年广西武鸣高中高二上学期段考化学(理)试卷 题型:填空题
(l0分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.lmol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处
(4)请你再提出一个合理且比较容易操作的方案(药品可任取),作简明扼要表述。
查看答案和解析>>
科目: 来源:2011-2012学年广西桂林十八中高二上学期期中考试化学(文)试卷 题型:填空题
(10分)某化学研究性学习小组通过分组实验来探究盐酸与醋酸电离程度的差异,探究过程如下表:
(1)、若甲、乙两组同学用pH试纸测溶液的pH时,均先用蒸馏水润湿pH试纸后再分别测定盐酸、醋酸、醋酸钠、氯化钠4种溶液的pH值,这种操作会导致上述所测的三种溶液的pH值出现偏差,不会出现偏差的溶液是 : ,测得溶液pH>7的有: 。
(2)、丙组实验中的两种溶液反应后,收集到的气体体积__(填“相等”或“ 不相等”)。
不相等”)。
(3)、以上3组实验中能证明醋酸是弱酸的是:_ 及 丙 组(填“甲”、“乙”或“丙”,下同),能证明盐酸是强酸的是__组。
查看答案和解析>>
科目: 来源:2011-2012学年内蒙古呼伦贝尔市牙克石林业一中高二上学期期中考试化学试卷 题型:填空题
(4分)25℃、1.01×105Pa时,氢硫酸饱和溶液的浓度为0.1mol·L-1,氢硫酸溶液呈酸性,用方程式表示主要原因 。向溶液中加入少量Na2S晶体,振荡后溶液的pH将 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源:2011-2012学年广东省佛山市罗村高级中学高二上学期第二阶段考试化学试卷 题型:填空题
(12分)在稀氨水中存在下述电离平衡NH3 + H2O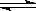 NH3 ·H2O
NH3 ·H2O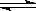 NH4+ + OH—,分别加入少量下列物质,溶液中c ( OH—) 如何变化?(填
NH4+ + OH—,分别加入少量下列物质,溶液中c ( OH—) 如何变化?(填 “增大”“减小”或“不变”);平衡移动方向如何(填“正向”或“逆向”)?
“增大”“减小”或“不变”);平衡移动方向如何(填“正向”或“逆向”)?
加入 的物质 的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c( OH—)的变化 | | | |
| 平衡移动方向 | | | |
查看答案和解析>>
科目: 来源:2011-2012学年河北省涿州二中高二上学期期中考试化学试卷 题型:填空题
(14分)一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸的稀溶液。(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________,
②同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是_____ _____,
③当其c(H+)相同时,物质的量浓度由大到小的顺序为_____________________,
④当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序为______________________。
⑤当c(H+)相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气(相同状况),则开始时反应速率的大小关系是__________________,反应所需的时间的长短关系是__________________。
⑥将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为___ __________。
查看答案和解析>>
科目: 来源:2011-2012学年山东省济宁市重点中学高二上学期期中考试化学试卷 题型:填空题
(10分)25℃时,50mL0.1mol/L醋酸中存在下述平衡:
若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将 ,溶液中c(H+)将 (增大、减小、不变);
⑵加入一定量蒸馏水,平衡将 ,溶液中c(H+)将 (增大、减小、不变)
⑶加入少量0.1mol/L盐酸,平衡将 ,溶液中c(H+)将 (增大、减小、不变)
⑷加入20mL0.10mol/LNaCl,平衡将 ,溶液中c(H+)将 (增大、减小、不变)
查看答案和解析>>
科目: 来源:2011-2012学年河南省开封高中高二上学期期中考试化学试卷 题型:填空题
(10分)25℃时,50mL0.1mol/L醋酸中存在下述平衡:_______________________。若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将__________,溶液中c(H+)将__________(增大、减小、不变);
⑵加入一定量蒸馏水,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
⑶加入少量0.1mol/L盐酸,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
⑷加入20mL0.10mol/LNaCl,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com