
科目: 来源:2011-2012学年浙江省余姚中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(8分)在6份0.01 mol·L-1氨水中分别加入下列各物质:
| A.浓氨水 | B.纯水 |
| C.少量K2CO3固体 | D.少量浓H2SO4 |
查看答案和解析>>
科目: 来源:2011-2012学年河南省平顶山市高二下学期期末考试理科综合化学试卷(带解析) 题型:填空题
(8分)现有室温的①HCl ②H2SO4 ③CH3COOH三种溶液。
(1)若三种酸均为pH=2的溶液,它们的物质的量浓度由大到小的顺序是___________(用序号表示,下同),三种酸溶液各取1mL,分别加水到1000mL,pH最小的是________。
(2)若三种酸均为0.1mol·L-1的溶液,它们的pH由大到小的顺序是________,三种酸溶液各取1mL,分别加水稀释到1000mL,pH最小的是_________。
查看答案和解析>>
科目: 来源:2011-2012学年云南大理州宾川县第四高级中学高二4月月考化学试卷(带解析) 题型:填空题
(4分)下列溶液,c(H+)由小到大的排列顺序是 ,PH由小到大的是 。
①0.05mol/LH2SO4 ② 0.1mol/NH3·H2O ③ 0.1mol/CH3COOH ④0.05mol/Ba(OH)2
查看答案和解析>>
科目: 来源:2011-2012学年云南大理州宾川县第四高级中学高二4月月考化学试卷(带解析) 题型:填空题
(3分)写出下列物质的电离方程式:
(1)H2CO3
(2)NaHSO4
(3) NH3·H2O
查看答案和解析>>
科目: 来源:2011-2012学年浙江省宁波四中高二下学期期末考试化学试卷(带解析) 题型:填空题
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 Ka= 1.75×10-5
碳酸 Ka1= 4.30×10-7 Ka2 = 5.61×10-11
亚硫酸 Ka1= 1.54×10-2 Ka2 = 1.02×10-7
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = ;
碳酸的第一步电离比第二步电离 (填“容易” 或 “困难”)。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > >
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是 (填序号)
| A.c(CH3COO-) | B.c(H+) | C.醋酸的电离平衡常数 | D.醋酸的电离度 |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省扬州市安宜高中高二下学期期中考试化学试卷(带解析) 题型:填空题
(12分)⑴① NH3 ②SO3 ③Cl2 ④BaSO4 ⑤酒精 ⑥CH3COONH4 ⑦HClO ⑧Cu。
以上物质中属于非电解质的是 ,属于强电解质的是 。
⑵常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”),设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(填“<”、“=”、“>”)。
⑶在25℃时,有pH为a(a≤6)的盐酸和pH为b(b≥8)的NaOH溶液,取Va L该盐酸,与该NaOH溶液中和,需Vb LNaOH溶液。若a + b>15,则Va∶Vb = (填表达式),且Va Vb(填“>”“<”或“=”)
查看答案和解析>>
科目: 来源:2011-2012学年浙江省浙东北三校高二下学期期中联考化学试卷(带解析) 题型:填空题
(8分)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①________②(填“>”、“<”或“=”,下同);与完全相同的镁条发生反应,开始时的反应速率:①______ ②; 中和等量NaOH时消耗的体积:①________②;与足量的Zn反应生成H2的物质的量:① ________②。
中和等量NaOH时消耗的体积:①________②;与足量的Zn反应生成H2的物质的量:① ________②。
查看答案和解析>>
科目: 来源:2011-2012年海南省海南中学高二下学期期中考试理科化学试卷(带解析) 题型:填空题
(15分)、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA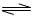 H++A―,则K=
H++A―,则K=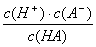 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。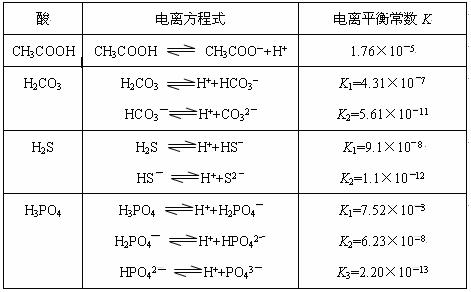
回答下列问题:
(1)当升高温度时,K值____(填“变大”“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最强的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是_____________,产生此规律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
查看答案和解析>>
科目: 来源:2011-2012学年海南省洋浦中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(9分)25℃时,有0.01 mol?L-1的醋酸溶液,试回答下列问题:
(1)写出醋酸的电离平衡常数表达式
(2)达平衡时,溶液中氢离子浓度是多少?(25℃时,醋酸的电离平衡常数为1. 75×10 -5)
(3)当向该溶液中加入一定量的盐酸时,溶液中的c(H+)、c (CH3COO-)、c (CH3COOH) 是否又发生变化? 电离常数是否发生变化? 为什么 ?
查看答案和解析>>
科目: 来源:2011-2012年浙江嵊泗中学高二下学期第二次月考化学试卷(平行班)(带解析) 题型:填空题
(10分)已知室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
(1)该溶液的pH=________;
(2)HA的电离平衡常数K=________;
(3)升高温度时,K将______(填“增大”、“减小”或“不变”),pH将______(填“增大”、“减小”或“不变”);
(4)由HA电离出的c(H+)约为水电离出的c(H+)的________倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com