
科目: 来源:2012-2013学年新疆兵团农二师华山中学高二上学期期末考试化学试卷(带解析) 题型:填空题
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<” )。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,
溶液中c(Na+) c(CH3COO-)
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。
(4)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
查看答案和解析>>
科目: 来源:2012-2013学年江苏省阜宁中学高二下学期期中考试化学试卷(带解析) 题型:填空题
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸(以下填空分别用a、b、c表示)
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是 。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是 。
(3) 将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是 。
(5)当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,则开始时反应速率的大小关系为 。
查看答案和解析>>
科目: 来源:2013届江西省南昌市高三上学期调研考试化学试卷(带解析) 题型:填空题
已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH) l.8 xl0-5,Ka(HSCN) 0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图。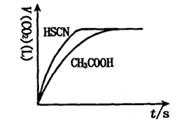
反应开始时,两种溶液产生CO2的速率明显不同的原因是 ;
反应结束后所得溶液中c(SCN-)____ c(CH3COO-)(填“>”,“=”或“<”)。
(2)2.0×l0-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如下图。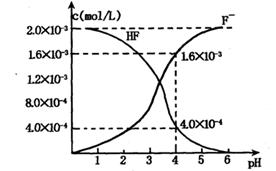
则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp= 1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4 mol/L的CaCl2溶液等体积混合,调节溶液pH =4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?____ (填“有”或“没有”),筒述理由: 。
查看答案和解析>>
科目: 来源:2010年6月浙江金华四校高二期末测试化学试题 题型:填空题
(6分)试回答下列问题(温度均为25℃时):
(1)将0. 2mol / L HB溶液与0.1 mol / LMOH溶液等体积混合,测得混合溶液的pH=4,则混合溶液中由水电离出的c(H+)__ __0. 2 mol / L HB溶液中由水电离出的c(H+)。(填“>”、“<”或“="”" )
(2)pH=13的Ba(OH)2溶液a L与pH=3的HCl溶液b L混合。若所得混合溶液呈中性,
则a∶b= ;
(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2 CO2=2 CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH--4e-=O2↑+2H2O则阴极反应式为________________________________。
查看答案和解析>>
科目: 来源:2009—2010学年沙河一中高二下学期化学单元测试(3) 题型:填空题
(3分)浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl溶液pH值由小到大的顺序是(填写编号)____________。
查看答案和解析>>
科目: 来源:2010届云南省曲靖一中高三高考冲刺卷(六)理科综合化学试题 题型:填空题
现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡_________移动(填“向左”,“向右”或“不”);其pH值变__________(填“增大”、“减小”或“无法确定”);另取10mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中 和
和 的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为: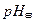 ______
______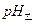 (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(3)各取25mL的甲、乙两溶液,分别用等浓度的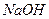 稀溶液中和至
稀溶液中和至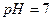 ,则消耗的
,则消耗的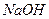 溶液的体积大小关系为:
溶液的体积大小关系为: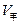 ______
______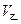 (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(4)取25mL的甲溶液,加入等体积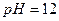 的
的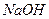 溶液,反应后溶液中
溶液,反应后溶液中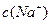 、
、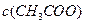 的大小关系为:
的大小关系为: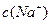 ______
______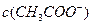 (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
查看答案和解析>>
科目: 来源:2010年上海市金山中学高一第二学期阶段质量检测化学试题 题型:填空题
下列四种溶液中,①pH=0的盐酸②0.1 mol·L-1的盐酸③0.01 mol·L-1的NaOH溶液④pH=11的NaOH溶液。由水电离生成的氢离子浓度之比是__________________。
查看答案和解析>>
科目: 来源:2010年山东省威海市高三第二次模拟考试(理科综合)化学部分 题型:填空题
(12分)运用相关原理,回答下列各小题:
Ⅰ.已知NaHSO4在水中的电离方程式为 NaHSO4=Na+ + H+ + SO42-。
(1)在NaHSO4溶液中c(H+) c(OH-)+ c(SO42-)(填 “>”、“=”或“<”下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH 7。
(2)将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为: ;向此反应后的溶液中滴加0.001 mol·L-1BaCl2溶液,首先析出的沉淀是 。[KSP(BaSO4)=1.1×10-10mol2·L-2;KSP(BaCO3)=5.1×10-9mol2·L-2]
Ⅱ.(1)工业上电解硫酸锌溶液可实现电解法炼锌(控制条件,使H+难放电、阳极电极不溶解)。写出相关的电解化学方程式: 。
(2)将干净的铁片浸在熔化的液体锌里可制得热镀锌铁板,这种铁板具有很强的耐腐蚀能力。镀锌铁板的镀锌层一旦被破坏后,锌将作为原电池的 极发生 反应而损耗,铁受到保护。
查看答案和解析>>
科目: 来源:湖南师大附中高二化学选修4结业考试理科试题 题型:填空题
(6分)从 、
、 、
、 、
、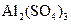 、
、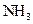 五种物质中:
五种物质中:
(1)选取溶于水中会促进水电离,且溶液显碱性的物质,用离子方程式表示溶液其显碱性的原因:
;
(2)选取溶于水会抑制水电离,且溶液显酸性的物质,用化学用语表示其显酸性的原因:
;
(3)选取溶于水会促进水电离,且溶液显酸性的物质,用离子方程式表示溶液其显酸性的原因:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com