
科目: 来源:2011-2012学年内蒙古巴彦淖尔市中学巴市一中高二上学期12月月考化学试卷 题型:实验题
如何防止铁的锈蚀是工业上研究的重要内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
| 序号 | 内容 | 实验现象 |
| 1 | 常温下将铁丝放在干燥空气中一个月 | 干燥的铁丝表面依然光亮 |
| 2 | 常温下将铁丝放在潮湿空气中一小时 | 铁丝表面依然光亮 |
| 3 | 常温下将铁丝放在潮湿空气中一个月 | 铁丝表面已变得灰暗 |
| 4 | 将潮湿的铁丝放在常温的氧气流中一小时 | 铁丝表面略显灰暗 |
| 5 | 将潮湿的铁丝放在高于常温的氧气流中一小时 | 铁丝表面已变得灰暗 |
| 6 | 将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 | 铁丝表面灰暗程度比实验5严重 |
查看答案和解析>>
科目: 来源:2011-2012学年江苏省无锡一中高二上学期期中考试化学试卷(必修) 题型:实验题
“阳光”牌小包装“脱氧剂”成份为Fe粉、活性炭及少量NaCl、水,使用一段时间后Fe粉会变质。某校化学兴趣小组欲探究使用过的 “脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行了如下探究过程,请你参与实验并回答有关问题。
步骤⑴取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末。由此得出的结论为上述“脱氧剂”中的铁已变质,发生了 腐蚀,生成的铁锈主要成分是 (填化学式);
步骤⑵将步骤⑴中的固体溶于水,过滤,将滤渣洗涤、干燥。该步骤的目的是 ;
步骤 ⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为 ;
⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为 ;
步骤⑷ 将步骤⑶中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全。为保证滤渣充分溶解,加入的稀H2SO4的体积应大于或等于 mL;
步骤⑸ 向步骤⑷中的混合物中加入过量的氢氧化钠溶液,得到的固体经洗涤后转移到坩埚中充分加热 ,冷却、称量,得到6.86g固体。
,冷却、称量,得到6.86g固体。
结论:该“脱氧剂”中的Fe粉的变质程度为 。
查看答案和解析>>
科目: 来源:2010年福建省养正中学、惠安一中、安溪一中高二上学期期中联考化学试卷 题型:实验题
Zn—MnO2干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 克。
查看答案和解析>>
科目: 来源:2013届山东省青岛二中高三上学期9月阶段性检测化学试卷(带解析) 题型:实验题
(8分)某化学研究小组以铜为电极电解饱和食盐水,探究过程如下:
实验1:如图所示连接装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30 s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10.随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,溶液始终未出现蓝色.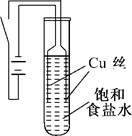
实验2:将实验1中试管底部的橙黄色沉淀取出,分装在两支小试管中,以后的操作和现象如下:
| 序号 | 操作 | 现象 |
| ① | 滴入稀硝酸溶液 | 沉淀溶解,有无色气泡产生,最终得到蓝色溶液 |
| ② | 滴入稀硫酸溶液 | 橙黄色沉淀转变为紫红色不溶物,溶液呈现蓝色 |
| 物质 | 颜色 | 物质 | 颜色 |
| 氯化铜 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 氢氧化亚铜(不稳定) | 橙黄色 |
| 碱式氯化铜 | 绿色 | 氢氧化铜 | 蓝色 |
| 氧化亚铜 | 砖红色或橙黄色 | 氯化亚铜 | 白色 |
查看答案和解析>>
科目: 来源:2011-2012学年河北广平县第一中学高二第二次调研考试理科化学试题(带解析) 题型:实验题
(共11分) 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题: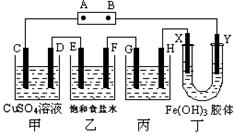
(1)电源A 极的名称是___________
(2)乙装置中电解反应的总化学方程式是________________
(3)如果收集甲、乙装置中C、D、E、F产生的物质的物质的量之比是________
(4)欲用丙装置给铜镀银,G应该是_____(填名称),电镀液的主要成分是______(填化学式)
(5)装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带_________电荷。
(6)从Cu2+、Na+、SO42-、Cl-四种离子中恰当地组成电解质,按下列要求进行电解,
写出所有符合要求的物质化学式。
①、以石墨为电极进行电解,使电解质质量减少,水质量不变,采用的电解质是________
②、以石墨为电极进行电解,使电解质质量不变,水质量减少,采用的电解质是________
③、以碳棒为阳极,铁棒为阴极进行电解,使电解质和水的质量都减少,采用的电解质是___
查看答案和解析>>
科目: 来源:2011-2012学年北京市101中学高二下学期期中考试化学试卷(带解析) 题型:实验题
(9分)利用下图电解装置进行实验。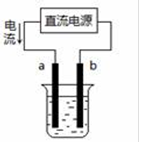
(1)若a、b是惰性电极,电解质溶液是氯化钠溶液,a极是 极,总反应的离子方程式是 。
(2)若a、b是惰性电极,电解质溶液是硝酸银溶液,b极上的现象是 ,总反应的离子方程式是 。
(3)若a、b是惰性电极,电解质溶液是硫酸钾溶液,a极上的电极反应是 ,若两极附近分别加入石蕊试液,两极附近的现象是 。
查看答案和解析>>
科目: 来源:2011-2012学年山西省“晋商四校”高二下学期联考化学试卷(带解析) 题型:实验题
(9分)某化学学习小组欲设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(预计H2的体积6mL左右)同时检验氯气的氧化性。现有以下的仪器可供选择:
(1)若要完成以上的实验,将所给仪器连成一整套装置,各种仪器接口的连接顺序(填编号)是:
A接 、 接 ,B 接 、 接 。
( 2)能说明氯气具有氧化性的实验现象是 。
(3)已知氯气溶于水中有如下平衡:Cl2+H2O HC1+HC1O。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸入40mLCl2和l0mL H2O。
HC1+HC1O。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸入40mLCl2和l0mL H2O。
①若将此针筒长时间放置在有日光的地方,最终可能观察到的现象是 。
②用化学平衡的观点解释①的现象:
(4)假定装入的饱和食盐水为50mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6mL(标准状况)时停止通电。摇匀U形管内的溶液后溶液的pH约为__ __。
查看答案和解析>>
科目: 来源:2011-2012年浙江温州龙湾中学高一期中考试理科化学试卷(带解析) 题型:实验题
(12分)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a,X、Y都是惰性电极,通过导线与直流电源相连。请回答以下问题:
⑴若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两极各滴入几滴酚酞试液,则
①写出电解饱和NaCl溶液的化学方程式
②电解池中X极附近观察到的现象是 。
③Y电极上的电极反应式为 ,
检验该电极反应产物的方法是 。
⑵如果用电解法精炼铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为
②Y电极的材料是 ,电极反应式主要为
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目: 来源:2012届四川省雅安中学高三下学期阶段测试理综试卷化学部分(带解析) 题型:实验题
.(16分)某课外活动小组同学用下图装置进行实验,试回答下列问题。
(1)若开始时开关K与a连接,则B极的电极反应式为 。
(2)若开始时开关K与b连接,则B极的电极反应式为 ,总反应的离子方程式为 ,有关该实验的下列说法正确的是(填序号) 。
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,设想用下图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为 。此时通过阴离子交换膜的离子数 (填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从 出口 (填写“A”、“B”、“C”、“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因 。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
查看答案和解析>>
科目: 来源:2011-2012学年甘肃武威六中高二上学期期末考试化学(理)试卷 题型:实验题
(12分)课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
(1)电源A 极的名称是___________
(2)甲装置中电解反应的总化学方程式是____________________________
(3)如果收集乙装置中产生的气体,两种气体的体积比是__________。
(4)欲用丙装置给铜镀银,G应该是___(填“铜”或“银”),电镀液的主要成分是 (填化学式)。
(5)装置丁中的现象是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com