
科目: 来源: 题型:单选题
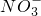 ,
,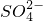 中各不相同的四种离子,若单独排放仍会造成环境污染,如果两厂的污水按适当比例混合,经沉淀后污水变成硝酸钠溶液,下列判断正确的是
中各不相同的四种离子,若单独排放仍会造成环境污染,如果两厂的污水按适当比例混合,经沉淀后污水变成硝酸钠溶液,下列判断正确的是查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
 Cu2++SO2↑+2H2O
Cu2++SO2↑+2H2O查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
| NaCl | NaHCO3 | NH4Cl | |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
| b∕a的取值范围 | 溶质 | 溶质物质的量 |
| ______ | ______ | ______ |
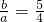 | -- | -- |
| ______ | ______ | ______ |
| ______ | ______ | ______ |
查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| B | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 乙醇(乙酸) | NaOH溶液 | 蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com