
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:单选题
| 操作及现象 | 解释 | |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,褪色 | SO2具有漂白性 |
| B | 配制FeCl3溶液时需加入少量盐酸 | 盐酸能抑制Fe3+的水解 |
| C | 某钠盐溶液中加入盐酸酸化的硝酸钡溶液有白色沉淀 | 说明该钠盐是硫酸钠或硫酸氢钠 |
| D | 向含有少量的FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
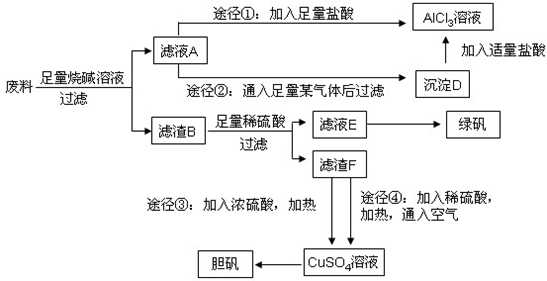
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com