
科目: 来源: 题型:解答题
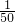 ,也可造成人的智力损伤.
,也可造成人的智力损伤.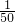 ,则吸入肺部CO的浓度不能超过______ mol?L-1.
,则吸入肺部CO的浓度不能超过______ mol?L-1. 中NO(g)、CO(g)、N2(g)的物质的量浓度变化如图所示,则反应进行到15min时,NO的平均反应速率为______;
中NO(g)、CO(g)、N2(g)的物质的量浓度变化如图所示,则反应进行到15min时,NO的平均反应速率为______;查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 物质 | 所用试剂 | 方法 |
| A | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 蒸馏 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
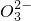 、Cl-
、Cl-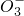 、C
、C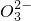
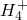 、S
、S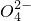 、Cl-
、Cl-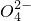 、N
、N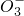
查看答案和解析>>
科目: 来源: 题型:多选题
| 第1份 | 第2份 | |
| 混合物质量(g) | 9.2 | 18.4 |
| 反应后固体质量(g) | 8.3 | 15.6 |
查看答案和解析>>
科目: 来源: 题型:单选题
 用如图表示的一些物质或概念间的从属关系中,不正确的是
用如图表示的一些物质或概念间的从属关系中,不正确的是| X | Y | Z | |
| A | 甘油 | 化合物 | 纯净物 |
| B | 胶 体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
查看答案和解析>>
科目: 来源: 题型:单选题
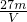 mol?L-1
mol?L-1 mol?L-1
mol?L-1 mol?L-1
mol?L-1 mol?L-1
mol?L-1查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com