
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 N2+3Cu+3H2O
N2+3Cu+3H2O NaCl+N2↑+2H2O.
NaCl+N2↑+2H2O.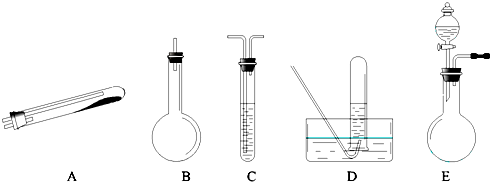
查看答案和解析>>
科目: 来源: 题型:单选题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 适量二氧化碳通入氯化钡溶液中 | 产生沉淀 | 碳酸的酸性比盐酸弱 |
B | 二氧化硫通入溴水中 | 溶液褪色 | 二氧化硫有漂白性 |
| C | 取少量某无色溶液,先滴加氯水,再加入少量四氯化碳,振荡、静置 | 溶液分层,下层呈橙红色 | 原无色溶液中一定有溴离子 |
D | 将铜片放入浓硝酸中 | 产生大量无色气体,溶液变为蓝绿色 | 只体现浓硝酸的强氧化性 |
查看答案和解析>>
科目: 来源: 题型:解答题
 A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.查看答案和解析>>
科目: 来源: 题型:单选题
 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示.则溶液中Fe(NO3)3、Cu( NO3)2、HN03物质的量浓度之比为
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示.则溶液中Fe(NO3)3、Cu( NO3)2、HN03物质的量浓度之比为查看答案和解析>>
科目: 来源: 题型:单选题




查看答案和解析>>
科目: 来源: 题型:解答题
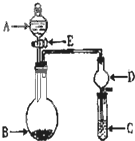 1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL
1、实验室要配制物质的量浓度为0.1mol/L的NaOH溶液480mL| 配制时应称量 NaOH的质量/g | 已给仪器 | 配制时除已给仪器外 还需要的其他仪器 |
| ______ | 烧杯、药匙、 托盘天平 | ______ |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com